Анемия Минковского-Шоффара: причины, симптомы, диагностика, лечение. Анемия минковского шоффара
Болезнь Минковского-Шоффара: причины, последствия, лечение
 Болезнь Минковского-Шоффара – это наследственная патология, которая может проявляться у детей раннего возраста. Основным проявлением этого заболевания является развитие анемии (малокровие), вследствие преждевременного разрушения большого количества дефектных эритроцитов в селезенке. Частота этой патологии составляет 2-3 случая на 10000 родившихся детей.
Болезнь Минковского-Шоффара – это наследственная патология, которая может проявляться у детей раннего возраста. Основным проявлением этого заболевания является развитие анемии (малокровие), вследствие преждевременного разрушения большого количества дефектных эритроцитов в селезенке. Частота этой патологии составляет 2-3 случая на 10000 родившихся детей.
Причины и механизм развития
Эритроциты имеют размер 7-8 мкм и форму двояковогнутого диска. Это дает им возможность свободно проходить в капиллярах (самые мелкие сосуды, через стенку которых происходит газообмен в тканях и их питание). При болезни Минковского-Шоффара (микрсфероцитоз) вследствие дефекта гена, нарушается синтез клеточной стенки эритроцитов, в ней уменьшается количество белка спектирна. Это вызывает усиленное поступление ионов натрия и воды внутрь эритроцита, что приводит к их «раздуванию». Они приобретают сферическую форму и теряют эластичность. В момент прохождения такого эритроцита через сосуды (синусы селезенки) он повреждается и через несколько таких прохождений разрушается. Это приводит к уменьшению количества эритроцитов и развитию гемолитической анемии. Такой дефектный ген может передаваться ребенку от 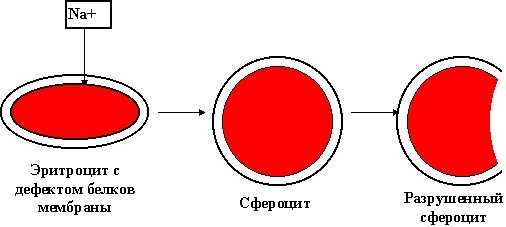
- Воздействие ионизирующего излучения (радиация, рентгеновские лучи).
- Попадание в организм развивающегося плода химических веществ, влияющих на геном его клеток (соли тяжелых металлов, циклические углеводороды, медикаменты, алкоголь, никотин, наркотические вещества).
- Инфицирование организма плода – в частности при вирусной инфекции ДНК вируса встраивается в геном клеток и приводит к мутации их генов.
Все эти провоцирующие факторы могут привести к формированию и других пороков развития, поэтому женщине необходимо максимально стараться ограничивать их воздействие.
Селезенка в физиологическом отношении является своеобразным «кладбищем эритроцитов», именно в ней происходит утилизация эритроцитов по окончанию срока их жизни, который в среднем длится 90-120 дней.
Симптомы
Проявления патологии зависят от степени выраженности и количества измененных эритроцитов. В большинстве случаев первичные симптомы проявляются у ребенка дошкольного и раннего школьного возраста. Течение микросфероцитоза волнообразное. Для него характерно наличие гемолитического криза (одновременное разрушение большого количества эритроцитов) и межприступного периода. Основным клиническим проявлением межприступного периода болезни или синдрома Минковского-Шоффара являются признаки анемии, к которым относятся бледность кожи, слизистых и склер глаз, небольшая их желтушность. Гемолитический криз характеризуется такими клиническими проявлениями:
- Желтуха – желтушно-зеленоватое окрашивание кожи, слизистых, вследствие увеличенного количества в крови
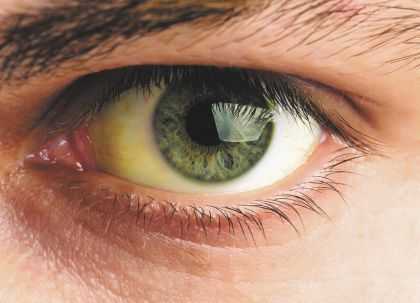
- Повышение температуры тела до +38° С, головная боль, общая слабость.
- Боль в животе, которая может иметь спастический характер.
- Боль в области печени (правое подреберье) вследствие ее увеличения.
- Увеличение в размерах селезенки.
Наличие таких симптомов и их выраженность определяются количеством разрушенных эритроцитов.
Иногда длительное время такая патология эритроцитов может себя абсолютно ничем не проявлять. Единственным симптомом в таких случаях является едва заметная желтушность кожи и склер, имеющая зеленоватый оттенок.
Осложнения и последствия
Тяжелая форма синдрома Минковского-Шоффара в раннем детском возрасте, длительная анемия может привести к отставанию ребенка в психическом и соматическом развитии, которое в дальнейшем практически невозможно исправить. Поэтому очень важным моментом в успешном лечении этой патологии является раннее выявление патологического процесса.
Диагностика
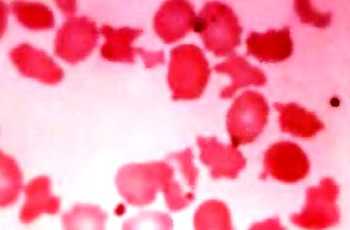
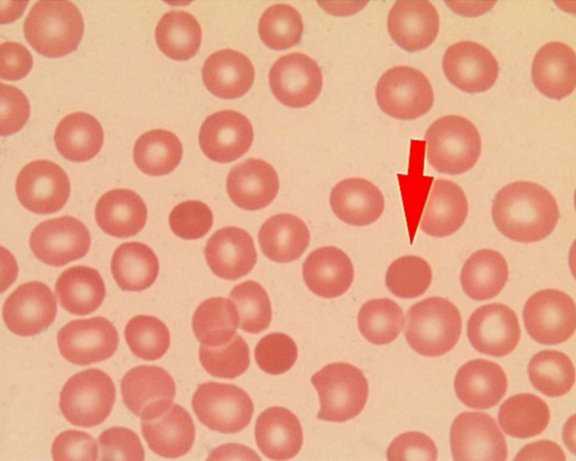 Диагностика этого заболевания является несложной. В клиническом анализе крови при микроскопии мазка, окрашенного по Романовскому-Гимзе, определяются измененные эритроциты в виде небольших сфер. Они теряют форму двояковогнутого диска. Для определения тяжести течения заболевания, проводится подсчет измененных форм с подсчетом их отношения к общему числу эритроцитов. Клинически значимым является течение патологии, при котором микросфероциты составляют 10-20% от общего числа эритроцитов.
Диагностика этого заболевания является несложной. В клиническом анализе крови при микроскопии мазка, окрашенного по Романовскому-Гимзе, определяются измененные эритроциты в виде небольших сфер. Они теряют форму двояковогнутого диска. Для определения тяжести течения заболевания, проводится подсчет измененных форм с подсчетом их отношения к общему числу эритроцитов. Клинически значимым является течение патологии, при котором микросфероциты составляют 10-20% от общего числа эритроцитов.
Для своевременной диагностики болезни Минковского-Шаффара и других заболеваний системы крови, рекомендуется проводить профилактический анализ крови ребенку один раз в год.
Лечение
Лечебная тактика зависит от тяжести процесса. В межприступном периоде и легком течении микросфероцитоза, активные терапевтические мероприятия не проводятся. Во время развития приступа гемолитической анемии, ребенок госпитализируется в стационар, где проводится дезинтоксикационная терапия, направленная на выведение продуктов распада гемоглобина (билирубин) из организма, скорейшее восстановление количества эритроцитов (витамины, препараты железа). Тяжелое течение с большим количеством микросфероцитов требует проведения операции спленэктомии (удаление селезенки). При этом количество измененных эритроцитов не уменьшается, но уже не происходит их разрушение при прохождении через селезенку. Такой вариант является методом радикальной терапии болезни Миковского-Шоффара.
Прогноз при болезни Минанковского-Шоффара благоприятный при раннем выявлении патологии и своевременном лечении, особенно это касается предотвращения развития анемии, которая сказывается на дальнейшем развитии ребенка.
prof-med.info
причины, симптомы, диагностика, лечение — Симптомы
Анемия долгое время считалась болезнью бедных людей: развиться недугу помогает отсутствие полезной пищи, простых необходимых витаминов, неблагоприятные окружающие условия. Казалось бы, подобные проблемы легко можно решить и анемия вообще должна кануть в Лету, однако статистика показывает неутешительные факты: каждый пятый ребёнок стоит на пороге этого заболевания. Беременные женщины попадают под удар первыми. Практически у каждой будущей мамочки врачи констатируют пониженный гемоглобин, а это – первая стадия болезни. Можно отмахнуться от всяких страхов, если бы не последствия, оставляемые анемией: у беременных – риск аномалии будущего малыша; у детей – изменения в составе крови, отрицательно влияющие на дальнейшее развитие; взрослым грозит потеря трудоспособности. Правильное лечение может остановить недуг, уничтожить его, но некоторые формы анемии не являются столь безобидными и простыми. Наследственный сфероцитоз, или анемия Минковского-Шоффара, относится именно к такой категории.
Первые упоминания об анемии относятся к эпохе Средневековья: бледные, измождённые лица считались эталоном красоты, слабость мышц только приветствовалась, особенно у прекрасных дам. Печальным итогом стремления к красоте была скорая смерть. В XIX веке учёные смогли выявить причину возникновения болезни. К тому времени анемия стала настоящей эпидемией, появились различные её формы, смертность от неё была достаточно высокой. В 1900 году немецкий врач-терапевт Оскар Минковский обнаружил, что анемия передаётся по наследству, а спустя 7 лет французский врач Анатоль Шоффар, продолжая исследования коллеги, окончательно разобрался с данным видом заболевания. Это довольно редкий тип: из 10 000 людей недуг поражает 3 – 4 человек. Болезнь предпочитает страны Европы, однако это не умаляет её опасности, ведь основной фактор – наследственность – подобен бомбе замедленного действия. Именно поэтому необходимо иметь элементарные знания об этой болезни.
Знакомство с анемией
Прежде всего, следует знать: анемия – заболевание кровеносной системы, поражающее красные кровяные клетки, эритроциты. Дефицит этих маленьких клеток приводит к различным нарушениям, сбоям, аномалиям в организме людей. Эритроциты и лейкоциты – главные кирпичики, из которых строится кровеносная система человека. Если лейкоциты выполняют защитную функцию, то, благодаря эритроцитам, происходят следующие важные процессы:
- насыщение всех органов кислородом;
- перенос углекислого газа из тканей, органов, мышц обратно в лёгкие;
- аминокислоты попадают во все участки тела, пополняя нужный уровень.
Другими словами, благодаря достаточному количеству эритроцитов, поддерживается вся работа организма, а вот нарушение баланса и дефицит красных клеток приводят к плачевным последствиям. «Рождаются» красные клетки в костном мозге, там же они проходят несколько этапов «взросления», необходимых для полноценного функционирования. Гомопоэтические клетки проходят следующие стадии:
- Мегалобласты.
- Эритробласты.
- Нормоциты.
- Ретикулоциты.
Между последним этапом развития клетки и моментом её появления проходит всего несколько часов. Главная составляющая эритроцита – всем известный гемоглобин, именно он отвечает за цвет этих клеток. Длительность «жизни» красных клеток невелика, всего лишь 60 – 120 дней, потом они попадают в печень или селезёнку, где происходит их разрушение. Количество красных кровяных клеток не должно уменьшаться. Как только умирают старые клетки, на подходе появляются новые. Таким образом тело человека функционирует правильно и чётко. Нормальная клетка напоминает красный двояковогнутый диск симметричной формы, состоящий из воды и гемоглобина. Нарушения внешнего вида эритроцита дают основания заподозрить отклонения, заболевания, мутации кровеносной системы.
Анемия поражает красные клетки, не давая им пройти весь процесс созревания. Как итог эритроциты погибают в костном мозге, не выполняя своих прямых обязанностей. Уровень красных телец резко падает, органы перестают получать столь нужный кислород. Отсюда появляются всем известные бледность кожи и слабость мышц. Более тяжёлые формы недуга изменяют саму клетку, а соответственно, и её функции. Кроме того, по причине изменения ДНК болезнь передаётся по наследству.
Причины и симптомы развития болезни
Микросфероцитарная анемия, выявленная Минковским и Шоффаром, получила своё второе имя в 1968 году. Составляющая эритроцита – мембранный белок энзим – под воздействием определённых факторов мутирует, в дальнейшем уничтожая другую составляющую – спектрин. Именно спектрин отвечает за форму и рост эритроцита, при его отсутствии красная клетка превращается в двояковыпуклую мелкую клетку. Таким образом родился термин «микросфроциты» – изменённые красные кровяные тельца. Маленькие мутанты в дальнейшем трансформируют остальные клетки, которые гибнут, не вызревая. Так начинается процесс, именуемый наследственным сфероцитозом.
Анемию Минковского-Шоффара обнаруживают у новорожденных при первом анализе крови. Родители сразу оказываются в шоковом состоянии, ведь им сообщают, что болезнь передалась от кого-либо из них. Аутосомно-доминантный тип зачастую присутствует у родственников маленького пациента. В большинстве случаев передача испорченного гена происходит по мужской линии, причём поражение клеток в дальнейшем будет прогрессировать. Процесс гемолиза – распада, гибели эритроцитов – начинается уже через несколько дней. Новые клетки не успевают родиться, организм не получает столь необходимых ему веществ, а главное – кислорода. Ситуацию ухудшают инфекции, неправильный образ жизни, злоупотребление алкоголем, наличие паразитов. Подобные факторы приводят к развитию гемолитического криза. Болезнь может прибрести злокачественную форму.
Наследственный тип заболевания делится на лёгкую и тяжёлую формы. Лёгкий тип анемии определяется последующими симптомами:
- желтуха лёгкой формы;
- увеличенные размеры селезёнки, печени, так как именно в этих органах происходит процесс отмирания красных кровяных клеток;
- бледная кожа;
- общая слабость;
- наличие камней в жёлчных протоках.
Тяжёлую форму заболевания характеризуют:
- высокая температура;
- серый или лимонный оттенок кожи;
- сильная слабость, потеря сознания, неспособность двигаться;
- значительно увеличенные селезёнка, печень, поджелудочная железа, соответственно, сильные боли в животе, боках;
- тошнота, рвота;
- изменение цвета кала, мочи;
- низкий показатель гемоглобина.
Иногда симптомы могут возникнуть в результате сильного стресса, например, после переохлаждения. Чем позже появляются первые признаки, тем тяжелее протекает наследственный сфероцитоз. Распадаясь, изменённые эритроциты вырабатывают большое количество билирубина. Не успевая выводиться из организма, он отрицательно влияет на многие органы. Именно этот компонент играет роковую роль. Особенно страдают от его токсического воздействия на нервную и половую системы маленькие дети. Это выражается в задержках умственного развития, мутациях физического плана, неправильном развитии органов.
Анемию не всегда удаётся распознать на её первых стадиях: порой единственным признаком является бледная, серая, жёлтая кожа, а поставить окончательный диагноз могут только специальные анализы: УЗИ брюшной полости, костно-мозговая пункция. Более тяжёлые формы оставляют значительный отпечаток на внешнем виде пациента: изменяется форма черепа (башенная), расширяется переносица, трансформируется нёбо, присутствует широкая щель между зубами.
Передача повреждённого гена может быть не только от отца к сыну – возможны варианты передачи болезни через поколение. Большую роль при этом играют образ жизни, питание, наличие вредных привычек, химическое воздействие на организм. Подобные факторы только усугубляют ситуацию, провоцируя более глубокие изменения в ДНК.
Что такое анемия?
Под анемией принято понимать состояние организма, характеризующееся резким снижением показателей эритроцитов и гемоглобина. Некоторые разновидности заболевания приводят к изменению формы красных кровяных клеток. С течением времени они утрачивают первоочередные функции.
Анемия часто сопровождает различные заболевания, но никогда не бывает первичной. Именно поэтому не стоит оставлять расстройство без внимания. Необходимо как можно быстрее найти его причину и постараться устранить.
Особенности гемолитической анемии
Понятие «гемолитической анемии» включает в себя обширную группу заболеваний. Все они характеризуются общим патогенезом. Усиленное разрушение эритроцитов приводит к увеличению продуктов их распада и к нарастанию эритропоэза. Цикл формирования красных телец нарушается. Процессы их разрушения постепенно начинают превалировать над механизмами появления и вызревания.
Все гемолитические анемии условно подразделяются на две группы: наследственные и приобретенные. В этой статье мы более подробно остановимся на первом варианте. Если быть точнее, то рассмотрим, что представляет собой наследственная анемия Минковского-Шоффара.
В медицинских справочниках можно встретить несколько названий, описывающих патологический процесс. Это и микросфероцитарная анемия, и наследственный сфероцитоз, и болезнь Минковского-Шоффара. Чаще всего используется последнее наименование по фамилиям ученых-первооткрывателей.
Данное заболевание считается весьма распространенным (1 случай на каждые 5 тыс. населения). Диагностируется преимущественно у жителей Северной Европы. Первые признаки становятся заметны у детей в раннем возрасте. Если не приступить к лечению недуга своевременно, его течение негативно отразится на функционировании всего организма.
Причины и механизм развития болезни
Анемия Минковского-Шоффара сопровождается нарушением структуры и функций клеточной мембраны эритроцитов. В результате происходящих процессов они меняют свою форму на круглую, становятся хрупкими. Появляются первые признаки гемолиза — разрушения красных кровяных клеток с одновременным выделением гемоглобина.
У здорового человека эритроциты по своей форме напоминают двояковогнутый диск, благодаря чему они беспрепятственно передвигаются по сосудам. При анемии в мембране этих элементов синтез белка нарушается. Это приводит к проникновению жидкости внутрь клеток. По этой причине они меняют свою форму. Проходя через сосуды, эритроциты сильно деформируются, а через некоторое время начинают разрушаться. На фоне происходящих процессов уровень красных кровяных элементов резко падает, развивается гемолитическая анемия.
Если у одного из родителей ранее уже был диагностирован этот недуг, он обязательно перейдет по наследству ребенку. Крайне редко больные дети рождаются у совершенно здоровых мам и пап. В этом случае анемия развивается на фоне изменений в ДНК. Первичная генная мутация происходит еще во время внутриутробного развития плода. Обязательным условием развития болезни является воздействие на организм матери следующих факторов:
- радиация, рентгеновское излучение;
- интоксикация солями тяжелых металлов, наркотическими веществами, никотином;
- вирусная атака.
Под воздействием перечисленных факторов может возникнуть не только анемия Минковского-Шоффара, но и более серьезные патологии. Поэтому во время беременности женщина должна стараться оберегать свой организм.
Первые симптомы
Клиническая картина во многом определяется степенью тяжести патологического процесса и количеством измененных эритроцитов. Первые его симптомы можно наблюдать у детей дошкольного и раннего школьного возраста. Течение анемии этого вида обычно волнообразное. Приступы гемолитического криза, когда происходит одновременное разрушение большого числа эритроцитов, сменяются периодами затишья. При этом симптомы могут чуть отличаться.
Например, межприступный период болезни проявляется признаками анемии. Среди них можно выделить бледность кожных покровов, слизистых и склер глаз. При гемолитическом кризе клиническая картина видоизменяется и сопровождается следующими симптомами:
- Повышение температуры до 38 градусов, головная боль, общее недомогание.
- Развитие желтухи.
- Боль в животе, отличающаяся спастическим характером.
- Дискомфорт в области печени из-за ее увеличения.
- Воспаление селезенки.
Наследственная гемолитическая анемия Минковского-Шоффара встречается и у взрослых. Наиболее частой причиной обращения к врачу в этом случае служит желтушность кожных покровов. Однако в большинстве случаев этот недуг протекает бессимптомно. Пациенты узнают о его существовании случайно и обычно во время профилактического осмотра.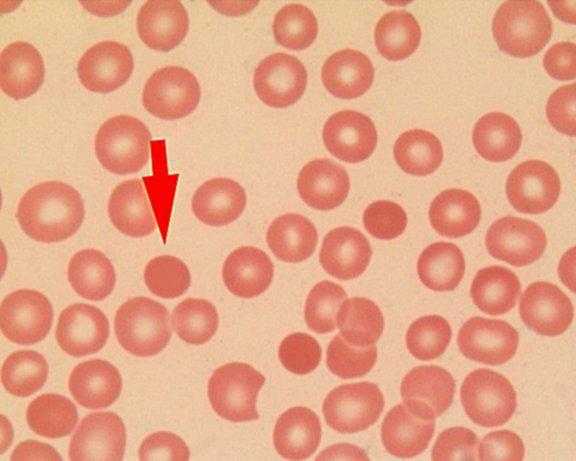
Медицинское обследование
Диагностика анемии Минковского-Шоффара достаточно проста. При подозрении на заболевание и появлении начальных его признаков следует обратиться за помощью к врачу. Патологии кроветворной системы находятся в компетенции гематолога. После изучения жалоб пациента и его семейного анамнеза специалист должен осмотреть кожные покровы и склеры, провести пальпацию живота. В обязательном порядке назначается УЗИ печени и селезенки, поскольку одним из симптомов недуга является увеличение в размерах этих органов.
Одновременно гематолог дает направление на ряд лабораторных анализов. Гемолитическая анемия Минковского-Шоффара подтверждается при наличии следующих изменений:
- Моча: гемоглобинурия, повышение показателей белка и уробилина.
- Биохимия крови: снижение холестерина, рост лактатдегидрогеназы, увеличение непрямого билирубина.
- Исследование эритроцитов: выраженный ретикулоцитоз, сокращение размеров клеток, понижение их осмотической устойчивости.
- Общий анализ крови: ускорение СОЭ, незначительное снижение тромбоцитов и лейкоцитов, сокращение цветового показателя.
Окончательно подтвердить предварительное заключение помогает проведение электрофореза белков мембраны эритроцита в сочетании с их количественным определением.
Дифференциальная диагностика
Гемолитическая анемия Минковского-Шоффара у детей иногда вызывает трудности во время диагностики. Это заболевание имеет схожие с другими аутоиммунными патологиями симптомы. Поэтому врачи должны знать некоторые отличительные и характерные именно для данного вида анемии признаки.
В первую очередь речь идет о наследственной предрасположенности. Только в исключительных случаях оба родителя оказываются абсолютно здоровыми. С другой стороны, у больного ребенка прослеживаются явные изменения в костях черепа. В сомнительных случаях дополнительно назначается проба Кумбса. Если анализ отрицательный, у пациента подтверждается анемия Минковского-Шоффара. Диагностика на этом считается завершенной.
Консервативные методы лечения
Терапия анемии подбирается с учетом ее тяжести. В период затишья, как правило, вмешательство не требуется. Во время очередного приступа больного сразу госпитализируют.
Консервативное лечение анемии Минковского-Шоффара включает в себя следующие меры воздействия:
- Заместительная терапия эритроцитарной массой, если уровень гемоглобина в крови падает до отметки 70 г/л.
- Лечение альбуминами назначается при высоких показателях билирубина.
- Для дезинтоксикации организма используется инфузионная терапия.
- В период отсутствия выраженного гемолитического криза показан прием желчегонных препаратов.
Продолжительность такой терапии, конкретные препараты и их дозировка — все эти вопросы решает врач в индивидуальном порядке.
Оперативное вмешательство
Если микросфероцитарная гемолитическая анемия Минковского-Шоффара протекает в тяжелой форме, консервативное лечение не справляется с заявленными задачами, пациенту рекомендуется операция по удалению селезенки. Такой подход не позволяет полностью вылечить недуг. С другой стороны, после вмешательства заметно сокращается число разрушенных эритроцитов, а их жизненный цикл удлиняется.
Гемолитические кризы после операции не повторяются, но она имеет ряд противопоказаний. Например, удаление селезенки не рекомендуется детям младше 5 лет по причине высокого уровня смертности в послеоперационный период. Негативной стороной процедуры считается снижение сопротивляемости организма по отношению к вирусным и грибковым инфекциям.
Альтернативным вариантом удаления селезенки считается эндоваскулярная окклюзия. Это еще один метод лечения, к помощи которого часто прибегают при диагнозе «микросфероцитарная анемия Минковского-Шоффара». В ходе процедуры врач вводит в орган лекарство, которое провоцирует спазм и приводит к инфаркту селезенки. Некоторая ее часть после этого сохраняет полноценное кровоснабжение и не утрачивает способность сопротивляться инфекциям.
Возможные осложнения
Гемолитическая анемия Минковского-Шоффара у детей дошкольного возраста часто приводит к отставанию в психическом и физическом развитии. Особенно если родители долго не обращались за медицинской помощью или игнорировали рекомендации врача.
У взрослых пациентов наиболее распространенным осложнением считается желчнокаменная болезнь на фоне нарушения билирубинового обмена. Все дело в том, что гемолитический криз часто воспринимают за начало развития механической желтухи, поэтому правильное лечение откладывается. При наличии камней в желчном пузыре рекомендуется проведение холецистэктомии вместе со спленэктомией.
Прогноз на выздоровление
При легком течении заболевания и своевременно проведенной операции по удалению селезенки прогноз благоприятный. Ремиссия обычно наступает сразу после гемолитического криза. Ее продолжительность может варьироваться, но в большинстве случаев составляет около двух лет.
Способы профилактики
Анемия Минковского-Шоффара носит наследственный характер. Поэтому предупредить возникновение заболевания не представляется возможным. В целях профилактики тяжелых форм недуга пациентам с выявленной формой анемии рекомендуется периодически проходить полное обследование у гематолога.
При планировании беременности следует понимать, что вероятность развития заболевания у будущего ребенка составляет 50%. Поэтому новорожденному также показано постоянное наблюдение у врача для выявления патологии на ранней стадии.
Причины и механизм развития
Эритроциты имеют размер 7-8 мкм и форму двояковогнутого диска. Это дает им возможность свободно проходить в капиллярах (самые мелкие сосуды, через стенку которых происходит газообмен в тканях и их питание). При болезни Минковского-Шоффара (микрсфероцитоз) вследствие дефекта гена, нарушается синтез клеточной стенки эритроцитов, в ней уменьшается количество белка спектирна. Это вызывает усиленное поступление ионов натрия и воды внутрь эритроцита, что приводит к их «раздуванию». Они приобретают сферическую форму и теряют эластичность. В момент прохождения такого эритроцита через сосуды (синусы селезенки) он повреждается и через несколько таких прохождений разрушается. Это приводит к уменьшению количества эритроцитов и развитию гемолитической анемии. Такой дефектный ген может передаваться ребенку от 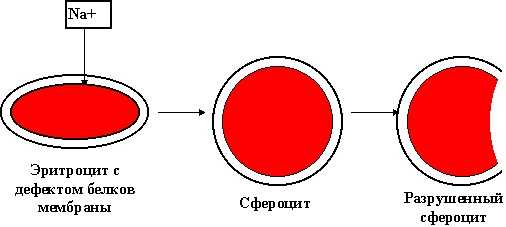 одного из родителей (в случае наличия у него такого же заболевания). Реже микросфероцитоз бывает результатом первичной мутации, когда оба родителя здоровые. Первичная мутация обычно происходит в процессе внутриутробного развития под действием провоцирующих факторов, к которым относятся:
одного из родителей (в случае наличия у него такого же заболевания). Реже микросфероцитоз бывает результатом первичной мутации, когда оба родителя здоровые. Первичная мутация обычно происходит в процессе внутриутробного развития под действием провоцирующих факторов, к которым относятся:
- Воздействие ионизирующего излучения (радиация, рентгеновские лучи).
- Попадание в организм развивающегося плода химических веществ, влияющих на геном его клеток (соли тяжелых металлов, циклические углеводороды, медикаменты, алкоголь, никотин, наркотические вещества).
- Инфицирование организма плода – в частности при вирусной инфекции ДНК вируса встраивается в геном клеток и приводит к мутации их генов.
Все эти провоцирующие факторы могут привести к формированию и других пороков развития, поэтому женщине необходимо максимально стараться ограничивать их воздействие.
Селезенка в физиологическом отношении является своеобразным «кладбищем эритроцитов», именно в ней происходит утилизация эритроцитов по окончанию срока их жизни, который в среднем длится 90-120 дней.
Симптомы
Проявления патологии зависят от степени выраженности и количества измененных эритроцитов. В большинстве случаев первичные симптомы проявляются у ребенка дошкольного и раннего школьного возраста. Течение микросфероцитоза волнообразное. Для него характерно наличие гемолитического криза (одновременное разрушение большого количества эритроцитов) и межприступного периода. Основным клиническим проявлением межприступного периода болезни или синдрома Минковского-Шоффара являются признаки анемии, к которым относятся бледность кожи, слизистых и склер глаз, небольшая их желтушность. Гемолитический криз характеризуется такими клиническими проявлениями:
- Желтуха – желтушно-зеленоватое окрашивание кожи, слизистых, вследствие увеличенного количества в крови
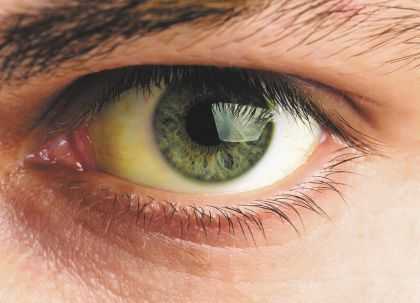 продуктов распада гемоглобина разрушенных эритроцитов.
продуктов распада гемоглобина разрушенных эритроцитов. - Повышение температуры тела до +38° С, головная боль, общая слабость.
- Боль в животе, которая может иметь спастический характер.
- Боль в области печени (правое подреберье) вследствие ее увеличения.
- Увеличение в размерах селезенки.
Наличие таких симптомов и их выраженность определяются количеством разрушенных эритроцитов.
Иногда длительное время такая патология эритроцитов может себя абсолютно ничем не проявлять. Единственным симптомом в таких случаях является едва заметная желтушность кожи и склер, имеющая зеленоватый оттенок.
Осложнения и последствия
Тяжелая форма синдрома Минковского-Шоффара в раннем детском возрасте, длительная анемия может привести к отставанию ребенка в психическом и соматическом развитии, которое в дальнейшем практически невозможно исправить. Поэтому очень важным моментом в успешном лечении этой патологии является раннее выявление патологического процесса.
Диагностика
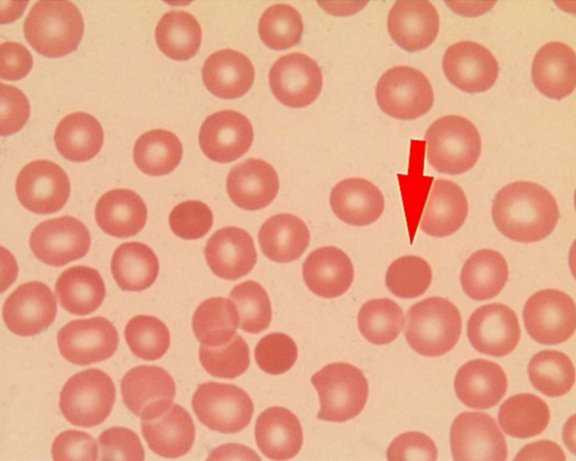 Диагностика этого заболевания является несложной. В клиническом анализе крови при микроскопии мазка, окрашенного по Романовскому-Гимзе, определяются измененные эритроциты в виде небольших сфер. Они теряют форму двояковогнутого диска. Для определения тяжести течения заболевания, проводится подсчет измененных форм с подсчетом их отношения к общему числу эритроцитов. Клинически значимым является течение патологии, при котором микросфероциты составляют 10-20% от общего числа эритроцитов.
Диагностика этого заболевания является несложной. В клиническом анализе крови при микроскопии мазка, окрашенного по Романовскому-Гимзе, определяются измененные эритроциты в виде небольших сфер. Они теряют форму двояковогнутого диска. Для определения тяжести течения заболевания, проводится подсчет измененных форм с подсчетом их отношения к общему числу эритроцитов. Клинически значимым является течение патологии, при котором микросфероциты составляют 10-20% от общего числа эритроцитов.
Для своевременной диагностики болезни Минковского-Шаффара и других заболеваний системы крови, рекомендуется проводить профилактический анализ крови ребенку один раз в год.
Лечение
Лечебная тактика зависит от тяжести процесса. В межприступном периоде и легком течении микросфероцитоза, активные терапевтические мероприятия не проводятся. Во время развития приступа гемолитической анемии, ребенок госпитализируется в стационар, где проводится дезинтоксикационная терапия, направленная на выведение продуктов распада гемоглобина (билирубин) из организма, скорейшее восстановление количества эритроцитов (витамины, препараты железа). Тяжелое течение с большим количеством микросфероцитов требует проведения операции спленэктомии (удаление селезенки). При этом количество измененных эритроцитов не уменьшается, но уже не происходит их разрушение при прохождении через селезенку. Такой вариант является методом радикальной терапии болезни Миковского-Шоффара.
Прогноз при болезни Минанковского-Шоффара благоприятный при раннем выявлении патологии и своевременном лечении, особенно это касается предотвращения развития анемии, которая сказывается на дальнейшем развитии ребенка.
simptomi.online
Анемия Минковского-Шоффара (наследственный микросфероцитоз) - патогенез, клиника
Анемия Минковского-Шоффара занимает не последнее место по распространённости среди всех анемий. На 10 000 человек приходится по некоторым данным от 2 до 4 пациентов с данным заболеванием. Попытки выявить причины данной анемии были предприняты ещё в 19 веке, однако тогда ещё трудно было установить, что патогенез заболевания скрывается в наследственном факторе, который обуславливает нарушение нормальной формы эритроцитов.
Этиология и патогенез анемии Минковского-Шоффара
Как известно, для нормального функционирования эритроцита необходимо поддержание его нормальной формы, иначе эритроцит просто не пройдёт через просвет сосуда. В поддержании двояковогнутой формы эритроцита участвует белок спектрин. При анемии Минковского-Шоффара имеется дефект синтеза данного белка. К тому же происходит нарушение работы АТФ-азы, ввиду чего возникает повышенное поступление натрия и воды в клетку. Это приводит к тому, что эритроцит приобретает форму сферы и имеет маленький размер. Из-за этого резко падает способность эритроцита восстанавливать свою структуру после прохождения сосудов, поэтому когда эти клетки крови проходят межсинусные пространства селезёнки, те из них, которые имеют патологическую форму, разрушаются. Из-за этого вместо 120 дней при наследственном микросфероцитозе эритроцит живет всего лишь 10.
Клиника анемии Минковского-Шоффара
Так как чаще всего анемия Минковского-Шоффара начинает проявляться ещё в детстве, на практике с ней наиболее часто сталкиваются педиатры. Наиболее важными симптомами заболевания являются анемия, желтуха, увеличение селезёнки, изменения скелета. Разрушение эритроцитов чаще происходит кризами, которые могут провоцироваться лекарствами, инфекциями. Для пациентов характерна бледность и желтушность кожных покровов, учащение сердцебиения и частоты дыхания, возможны тошнота и рвота, а также боли в животе. Со стороны скелета возможно изменение формы черепа, который приобретает вид башни, могут быть широко расставлены глаза, может наблюдаться картина готического нёба и нарушение зубного ряда.
При гемолитическом кризе отмечается низкий уровень гемоглобина (менее 70 г/л). Для анемии Минковского-Шоффара характерно снижение максимальной и минимальной осмотической стойкости эритроцитов, кривая Прайс-Джонса сдвинута влево. В окрашенных мазках крови микросфероциты определяются как интенсивно окрашенные клетки, не имеющие характерных для эритроцитов просветлений в центре. Билирубин в биохимическом анализе крови повышен в основном за счёт неконъюгированного.
Нужно отметить, что болезнь может протекать достаточно благоприятно годами. Иногда наследственный микросфероцитоз осложняется желчекаменной болезнью.
Лечение анемии Минковского-Шоффара
Лечение анемии Минковского-Шоффара при лёгкой и средней степени тяжести стараются вести консервативно. Для этого используют инфузионную терапию: растворы глюкозы, реополиглюкин, гемодеза. При тяжёлой степени проводят спленэктомию, оптимальным возрастом ребёнка для которой является 5-6 лет. В особых случаях приходится прибегать к переливанию эритроцитарной массы.
Для ребёнка с анемией Минковского – Шоффара важно соблюдать диету, щадящую печень, не нарушать режим труда и отдыха. Родителям такого необходимо объяснить целесообразность прививок, чтобы предотвратить вирусные и бактериальные инфекции.
12.08.2010
spravzdrav.ru
Анемия Минковского-Шоффара
27 августа 2015
Просмотров: 2213
Что такое анемия Минковского-Шоффара, как она проявляется? Эти вопросы интересуют многих пациентов. При слове «анемия» возникает ассоциация с «малокровием». Той или иной формой заболевания страдают очень многие, причем нужно знать, что в самостоятельном виде оно не существует. Чаще всего это состояние организма, при котором в крови отмечаются низкие показатели эритроцитов и гемоглобина.

Чаще всего анемия развивается в виде осложнения патологии и бывает разных типов. Например, недостаток витаминов группы В, Е, или С также называют словом «анемия». Однако видов анемии намного больше. Некоторые из них имеют аутоиммунную природу происхождения, их называют гемолитическими.
Анемия Минковского-Шоффара имеет свои особенности. Существует несколько причин, которые способствуют развитию этого состояния организма. Кроме того, существуют некоторые виды гемолитической анемии, которые имеют похожие симптомы.
Почему развивается микросфероцитарная анемия
Это заболевание имеет наследственное происхождение, оно связано с повреждениями белков, которые находятся в мембране эритроцитов.
Их форма становится сферической, что постепенно разрушает селезенку.
Согласно статистике, чаще всего этот вид анемии встречается на европейском континенте, реже — в Африке, заболевание диагностируется и в России.
Проявиться она может независимо от возраста, чаще — у детей и подростков, в группе риска находятся и близкие родственники. Очень часто носительство генов микросфероцитоза протекает бессимптомно.
Как передается микросфероцитарная гемолитическая анемия?
- Механизм передачи по наследству этого заболевания лежит в аутосомно-доминантном типе.
- Нередко диагностируется заболевание, которое передается по гетерозиготному принципу.
При анемии этого типа в мембранах эритроцитов появляются дефекты, которые развиваются в результате того, что в клетки поступают ионы натрия в большом количестве.
В клетках появляется избыточное количество воды, в итоге эритроциты принимают сферическую форму. Процесс разрушения структуры мембраны происходит под воздействием макрофагов селезенки, что объясняется нарушением кровообращения.
Как классифицируется анемия
Существует несколько форм гемолитической анемии, которые диагностируются у подростков и во взрослом возрасте.Заболевание проявляется следующими симптомами:
- общая слабость;
- повышенная утомляемость;
- головокружение;
- шум в голове;
- одышка;
- тахикардия при физической работе;
- кожа и склеры становятся желтыми;
- образование камней в желчном пузыре;
- болит печень;
- моча становится темного цвета;
- на голенях начинают образовываться трофические язвы;
- может развиться тромбоз;
- пигментация на коже;
- экзема;
- гемангиомы.
Если анемия выявлена еще в детском возрасте, то она протекает с выраженной симптоматикой, которая выражается в деформации скелета и костей черепной коробки.
Нормохромный тип анемии выражен пониженным гемоглобином 90-100 г/л. В состоянии криза, который происходит часто, гемоглобин становится еще ниже — 40-50 г/л. В некоторых случаях заболевание протекает в скрытой форме и может не сопровождаться анемией. При этом отмечается незначительный ретикулоцитоз и возникает реакция костного мозга эритробластического типа.
Таким образом, анемия Минковского-Шоффара является наследственным заболеванием, которое также называется врожденной гемолитической желтухой. Болезнь сопровождается гемолизом печени и селезенки.
Какие проявления характерны для анемии Шофара
Заболевание проявляется микросфероцитозом эритроцитов. Как правило, диаметр их становится небольшим, около 6,3 мкм, толщина значительно больше 2,1 мкм. В период обострения значительно сокращается продолжительность жизни эритроцитов. Распадаются они в области селезенки.
Нередко заболевание протекает в хронической форме, иногда даже состоянию глубокой анемии характерно бессимптомное течение. Очень часто появляется выраженная желтуха, при этом размеры селезенки и печени значительно увеличиваются. Для заболевания характерны регулярные обострения и фазы затухания.
Характерным признаком является появление мочи черного цвета. В зависимости от вида анемии, она может протекать в острой или в хронической форме. При холодовой гемагглютиновой анемии симптомы несколько иные: начинают синеть и белеть пальцы на руках и ногах, это приводит к нарушению периферического кровообращения, развивается тромбоз.
Для того чтобы определить развитие заболевания, врач назначает тесты и анализы крови. Для аутоиммунной анемии характерны макроцитоз и микросфероцитоз, нередко обнаруживаются нормобласты. Показатели СОЭ значительно увеличены. Если заболевание протекает в хронической форме, то лейкоциты образуются в пределах нормы. В период криза лейкоцитоз может быть на высоком уровне.
Полную ясность может внести только анализ крови. Очень часто заболевание протекает на фоне аутоиммунной тромбоцитопении. При этом нарушается и эритропоэз, чаще всего он усиливается. В кале появляется большое количество билирубина и стеркобилина. В том случае, если результат положительный, надо выявить, к какому классу относятся антитела.Характерным признаком анемии данного типа является микросфероз эритроцитов.
Как лечится гемолитическая анемия
Для лечения данной анемии используются гормоны, которые относятся к кортикостероидам. В том случае, если терапия неэффективна, назначается проведение операции на селезенке. Чаще всего ее удаляют. Основными показаниями являются:
- желтуха, которая продолжается длительное время;
- частые появления приступов желчекаменной болезни;
- частые обострения.
Единственным способом решить эти проблемы является спленэктомия.
На сегодняшний день этот способ является наиболее эффективным и применяется при лечении анемии, которая передается по наследству, или приобретенной. Однако при энзимопенической форме вмешательство не результативно или малоэффективно. Заболевание следует лечить, и подходить к этому вполне серьезно.
Чаще всего заболевание осложняется инфарктами и периспленитами, которые являются наиболее распространенным проявлением. Нередко они осложняются состоянием слабости и появлением анемичности. Характерными проявлениями являются трофические язвы в области голени.
Лечение трофических язв обычными способами не приносит никакого результата. Их образование происходит на фоне повышенного гемолиза. После проведения операции заживление язв происходит быстро. В легкой форме заболевание проявляется только незначительными косметическими дефектами. Если анемия протекает в тяжелой форме, то это может привести к инвалидности.
Автор:
Иван Иванов
Поделись статьей:
Оцените статью:
Загрузка...Похожие статьи
osostavekrovi.ru
Наследственный микросфероцитоз (болезнь Минковского — Шоффара)
В статье приведен обзор литературы, касающийся клинических и лабораторных проявлений, диагностики, лечения и прогноза наследственной микросфероцитарной анемии. Описаны результаты собственных наблюдений двоих пациентов, находящихся на лечении в онкогематологическом отделении Йошкар-Олинской детской городской больницы.
Hereditary microspherocytosis (Minkowsky — Shauffard disease)
The paper presents a literature review of clinical and laboratory manifestations, diagnosis, treatment and prognosis of hereditary microspherocytic anemia. It is describes the results of his own observations of two patients treated in oncohematological office in Yoshkar-Ola City Children’s Hospital.
Наследственный микросфероцитоз был впервые описан в 1900 году Минковским, а в дальнейшем более подробно — Шоффаром. Распространенность данного заболевания — 1:5000 населения, наиболее часто встречается у жителей Северной Европы [1, 2].
Патогенез. Врожденная микросфероцитарная гемолитическая анемия представляет собой семейное заболевание, наследуемое по аутосомно-доминантному типу. В основе заболевания лежит генетический дефект белка мембраны эритроцитов, в результате чего повышается ее проницаемость для ионов натрия, что приводит к набуханию эритроцитов, нарушению способности эритроцитов деформироваться, отщеплению в селезенке части их поверхности, укорочению продолжительности их жизни и разрушению макрофагами селезенки [3, 4]. Патология эритроцитов проявляется морфологической аномалией — микросфероцитозом. Продолжительность пребывания микросфероцитов в циркулирующей крови резко уменьшена, средний срок их пребывания в кровеносном русле может составлять 12-14 дней (вместо нормальных 120-125 дней) [5].
Клиническая картина. Центральное место в клинической картине принадлежит гемолитическому синдрому, который проявляется тремя кардинальными признаками: желтухой, спленомегалией и анемией [5]. Могут наблюдаться признаки замедленного развития, а также нарушение лицевого скелета в виде «башенного черепа», седловидного носа, высокого стояния неба, нарушение расположения зубов, узких глазниц [6]. Выраженность анемического синдрома различна. Часто наблюдается умеренное снижение гемоглобина. У некоторых больных анемия вообще отсутствует. Наиболее резкая анемизация наблюдается в период гемолитического криза. Микросфероцитарная гемолитическая анемия имеет хроническое течение и сопровождается периодическими кризами и ремиссиями. Гемолитический криз возникает под влиянием провоцирующих факторов (инфекция, переохлаждение, переутомление, беременность и другие) и проявляется резким усилением симптомов на фоне непрерывно текущего гемолиза [6]. При этом повышается температура в связи с массовым распадом эритроцитов, увеличивается интенсивность желтухи, выражена гепатомегалия, селезенка плотная и гладкая, нередко болезненная в результате напряжения капсулы при кровенаполнении или перисплените. Гемолитическая болезнь нередко осложняется приступами печеночной колики, вследствие образования пигментных камней в желчном пузыре и в желчных протоках. В связи с приступами печеночной колики и застоем желчи в печени у больных могут наблюдаться симптомы ангиохолецистита и паренхиматозного гепатита с появлением прямого билирубина в крови. При обострении болезни наблюдается наклонность к носовым кровотечениям [3, 7]. Несмотря на врожденный характер, болезнь лишь в редких случаях проявляется в первые дни после рождения, обычно симптомы проявляются в детском, чаще в 3-10 лет, или зрелом возрасте [8].
Лабораторная диагностика. При микроскопическом исследовании препаратов периферической крови выявляются сфероциты, характеризующиеся уменьшением значений среднего диаметра (меньше 7,2-7,0 мкм) на фоне нормального среднего объема МСV и увеличенного значения МСНС. Кривая распределения эритроцитов по размеру (кривая Прайс-Джонса) на графике смещена влево. Анемия носит нормохромный характер. Величина RDW превышает 12% (анизоцитоз). Ретикулоцитоз — 15%-30% [1, 10]. Число лейкоцитов обычно нормальное. При гемолитических кризах отмечается нейтрофильный лейкоцитоз со сдвигом влево. Количество тромбоцитов варьирует в пределах нормы. Содержание непрямого билирубина в крови повышено умеренно и, как правило, не превышает 50-70 мкмоль/л [6, 7]. Аутоантитела на мембране эритроцитов не выявляются, прямая проба Кумбса — отрицательная. Характерным лабораторным признаком является снижение осмотической резистентности эритроцитов по отношению к гипотоническим растворам хлорида натрия. Начало гемолиза при наследственном микросфероцитозе соответствует 0,6-0,7%, а конец — 0,4% вместо 0,48-0,22% в норме [1, 9]. Снижение осмотической резистентности свидетельствует о преобладании в крови эритроцитов сферической формы — сфероцитов, которые менее стойки к осмотическому гемолизу, чем нормальные макропланоциты (рис. 1).
Рисунок 1. Морфология микросфероцитов в мазках периферической крови больного (слева), здорового (справа)
Дифференциальная диагностика наследственного микросфероцитоза сводится к диагностике гемолитической анемии вообще. Многим больным ошибочно ставят диагноз синдрома Жильбера, хронического гепатита или даже цирроза печени, а анемию считают следствием этих заболеваний. Во всех случаях желтухи необходимо тщательное обследование больного независимо от содержания гемоглобина. Преимущественное увеличение содержания непрямого билирубина, ретикулоцитов, выявляемый при просмотре мазка микросфероцитоз дают основание для правильного диагноза. Затем необходима дифференциальная диагностика аутоиммунной гемолитической анемии и микросфероцитоза, так как аутоиммунные гемолитические анемии часто дают симптоматический микросфероцитоз [3]. В этой ситуации помогают тщательное выяснение анамнеза, давности заболевания, наличие подобного заболевания у родственников, выявление изменений скелета, постановка проб, позволяющих выявить аутоантитела (прямая проба Кумбса).
Лечение и прогноз. Лечение во время гемолитического криза направлено на ликвидацию анемии, гипоксии, гипербилирубинемии. Методом выбора при лечении наследственного сфероцитоза является спленэктомия, оптимальная в возрасте 4-5 лет. Спленэктомия обеспечивает практическое выздоровление, несмотря на сохранность сфероцитоза. Показанием к спленэктомии при микросфероцитозе являются постоянная или возникающая в виде кризов анемия, значительная гипербилирубинемия, даже без анемии, появление болей в правом подреберье, отставание в развитии у детей [3]. Переливания крови (эритроцитарной массы) показаны в случае тяжелого гемолитического криза [5]. Прогноз при наследственном микросфероцитозе благоприятный. Вероятность развития заболевания у детей, если один из супругов болен микросфероцитозом, несколько ниже 50% [9].
Клинический случай № 1. Больной С., 1 год 10 мес., с 01.06.09 г. по 09.06.09 г. находился на стационарном обследовании в онкогематологическом отделении Йошкар-Олинской детской городской больницы. Из анамнеза известно, что ребенок от первой беременности, родился недоношенным, с массой тела 900 грамм. Выхаживался в отделении второго этапа выхаживания недоношенных. Наследственность неизвестна, так как в четырехмесячном возрасте был усыновлен. С рождения отмечались снижение уровня гемоглобина в анализе крови, иктеричность кожных покровов. С декабря 2008 года наблюдается гематологом по поводу анемии недоношенных, принимал препараты железа. При поступлении жалобы на вялость, слабость, повышение температуры до фебрильных цифр, бледность и желтушное окрашивание кожных покровов. При пальпации печень выступает из-под края реберной дуги на 2,5 см, селезенка — на 2 см, мягкая, эластичная.
Общий анализ крови от 01.06.09 г.: HGB — 106 g/l, RBC — 3,9×10¹²/l, WBC — 11,6×109/l, Ht — 26%, MCV — 68,8 fl, MCH — 25,8 pg, МСНС — 375 g/l, RDW — 20,5%, PLT — 434×109/l, СОЭ — 6 мм/ч, в лейкоцитарной формуле: эозинофилы — 10%, с/я нейтрофилы — 34%, лимфоциты — 47%, моноциты — 9%.
Анемия носит нормохромный характер. В мазках крови преобладают микросфероциты, отличающиеся отсутствием характерного для нормальных эритроцитов центрального просветления, что подтверждается графически на кривой Прайс-Джонса, отражающей количественные соотношения эритроцитов различных диаметров. Вершина кривой Прайс-Джонса растянута и сдвинута влево в сторону микроцитов. Кроме того, в мазках крови просматриваются нормоциты и единичные макроциты, это подтверждает увеличение индекса RDW — 20,5%. Во многих эритроцитах определяется базофильная пунктация и полихроматофилия. Ретикулоцитоз — 27%. Осмотическая резистентность эритроцитов: min — 0,52%, max — 0,34% (при норме 0,48-0,22%) — определяется понижение резистентности по отношению к гипотоническим растворам поваренной соли. Биохимический анализ от 02.06.09 г.: концентрация непрямого билирубина — 29,9 мкмоль/л, АЛТ — 15 Е/л, АСТ — 26 Е/л, щел. фосфатаза — 415 Е/л, ЛДГ — 273 Е/л, показатели метаболизма железа в пределах нормы: сывороточное Fe — 14,4 мкм/л, ОЖСС — 69,9 мкм/л. Отрицательный результат прямой пробы Кумбса позволил исключить аутоиммунную гемолитическую анемию.
При наследственном микросфероцитозе картина крови характеризуется патологической триадой со стороны эритроцитов: 1) микросфероцитозом; 2) ретикулоцитозом; 3) пониженной осматической резистентностью. В нашем случае все три фактора хорошо выражены. Больному был выставлен диагноз «наследственная микросфероцитарная гемолитическая анемия».
Ребенок выписан в стабильном состоянии 09.06.09 г. с рекомендациями: наблюдение гематолога и педиатра, общий и биохимический анализы крови 1 раз в 3 месяца.
24.06.09 г. больной С. повторно поступает в онкогематологическое отделение. При поступлении состояние тяжелое, жалобы на вялость, отсутствие аппетита, плохой сон, повышение температуры до 39,6°С, бледность, желтушность кожных покровов, темный цвет мочи. Зев гиперемирован, рыхлый. Увеличены лимфатические узлы шейной группы. Живот увеличен в объеме, печень выступает из-под края реберной дуги на 3,5 см, селезенка — на 5 см.
Общий анализ крови от 24.06.09 г.: HGB — 89 g/l, RBC — 3,4×10¹²/l, WBC — 27,7×109/l, Ht — 21%, MCV — 68,6 fl, MCH-25,5 pg, МСНС — 381 g/l, RDW — 20,8%, PLT — 260×109/l, СОЭ — 12 мм/ч, в формуле: эозинофилы — 4%, базофилы — 1%, п/я нейтрофилы — 4%, с/я нейтрофилы — 15%, лимфоциты — 20%, моноциты — 1%, атипичные мононуклеары — 55%. Ретикулоцитоз — 46,7%. В мазках крови до 50% микросфероцитов. Непрямой билирубин — 41 мкмоль/л, АЛТ — 19 Е/л, АСТ — 45 Е/л, щел. фосфатаза — 316 Е/л, ЛДГ — 295 Е/л. Определяется повышенное содержание стеркобилина в кале. В моче отмечается уробилинурия, выделение уратов и кристаллов мочевой кислоты, объясняемое повышенным распадом эритроцитов. ИФА на вирус Эпштейна — Барр (инфекционный мононуклеоз) — положительный.
Учитывая у ребенка наличие интоксикации, лихорадки, увеличение шейных групп лимфоузлов, в крови высокий лейкоцитоз, мононуклеары до 55%, положительный ИФА, был диагностирован инфекционный мононуклеоз, который в свою очередь явился пусковым моментом для развития у мальчика гемолитического криза.
Проведено лечение: диета, постельный режим, инфузионная и противовирусная терапия. В результате терапии лихорадка купирована, уменьшились размеры печени, селезенки и лимфатических узлов. Общий анализ крови от 06.07.09 г.: HGB — 104g/l, RBC — 3,9×10¹²/l, WBC — 10,7×109/l, Ht — 28%, MCV — 73,3 fl, MCH — 26,4 pg, МСНС — 360 g/l, RDW — 21,8%, PLT — 452×109/l, СОЭ — 2 мм/ч, в лейкоцитарной формуле: эозинофилы — 5%, п/я нейтрофилы — 5%, с/я нейтрофилы — 25%, лимфоциты — 47%, моноциты — 8%, атипичные момонуклеары — 10%. Ретикулоцитоз — 9,3%. Количество микросфероцитов снизилось до 23%. Непрямой билирубин — 18,8 мкмоль/л. Нормализовались аппетит и сон. В стабильном состоянии 09.07.09 г. ребенок выписан домой с рекомендациями: наблюдение гематолога 1 раз в 3 месяца, общий анализ крови с ретикулоцитами и биохимический анализ крови 1 раз в 3 месяца, контроль УЗИ брюшной полости 1 раз в год.
Клинический случай № 2. Больная Г., 12 лет, 22.09.09 г. переведена в онкогематологическое отделение Йошкар-Олинской детской городской больницы из инфекционного стационара. При поступлении жалобы на заложенность носа, боль в горле, общую слабость, увеличение шейных и затылочных лимфоузлов, лихорадка до 39,2°С, иктеричность кожных покровов, гепатоспленомегалия с выраженной плотностью паренхиматозных органов. Из анамнеза известно, что отец девочки страдает синдромом Жильбера и у девочки с рождения на фоне повышения температуры, ОРВИ — появляется желтушность кожи, склер.
Общий анализ крови от 23.09.09 г.: HGB — 61g/l, RBC — 1,8×10¹²/l, WBC — 10,7×109/l, Ht — 16%, MCV — 85 fl, MCH — 32,5 pg, МСНС — 382g/l, RDW — 20,3%, PLT — 162×109/l, СОЭ — 48 мм/ч, в лейкоцитарной формуле: миелоциты — 1%, метамиелоциты — 2%, п/я нейтрофилы — 29%, с/я нейтрофилы — 9%, лимфоциты — 24%, моноциты — 4%, атипичные мононуклеары — 31%. Ретикулоцитоз — 82,5%. В мазках крови значительное количество микросфероцитов. Осмотическая резистентность эритроцитов: min — 0,72%, max — 0,42%, определяется резкое понижение резистентности по отношению к гипотоническим растворам поваренной соли. Повышено содержание уробилина в моче и стеркобилина в кале. Биохимический анализ крови от 23.09.09 г.: АЛТ — 71 Е/л, АСТ — 78 Е/л, ЛДГ 1234 Е/л, билирубин прямой — 5,68 мкмоль/л, непрямой — 54,8 мкмоль/л. Прямая проба Кумбса — отрицательная.
Тяжелая нормохромная анемия, обнаружение значительного количества микросфероцитов в препаратах крови, выраженный ретикулоцитарный криз, резкое понижение осмотической резистентности эритроцитов, гипербилирубинемия, а также наличие сходной симптоматики у отца дали основание диагностировать у девочки гемолитический криз наследственной микросфероцитарной анемии, спровоцированный инфекционным мононуклеозом (ИФА на вирус Эпштейна — Барр — положительный). Осмотр инфекциониста подтверждает диагноз инфекционного мононуклеоза.
Больной были назначены инфузионная, антибактериальная и противовирусная терапия, витамины. На фоне лечения состояние пациентки стабилизировалось. Общий анализ крови от 12.10.09 г. : HGB — 106g/l, RBC — 3,5×10¹²/l, WBC — 3,9×109/l, Ht — 29,3%, MCV — 83,8 fl, MCH — 30,4 pg, МСНС — 362 g/l, RDW — 217,8%, PLT — 170×109/l, СОЭ — 8 мм/ч, в формуле: базофилы — 1%, п/я нейтрофилы — 4%, с/я нейтрофилы — 62%, лимфоциты — 20%, моноциты — 4%, атипичные мононуклеары — 9%. Ретикулоцитоз — 13,1%. Биохимический анализ крови: АЛТ — 41 Е/л, АСТ — 32 Е/л, билирубин прямой — 2,75 мкмоль/л, непрямой — 24,35 мкмоль/л. По данным УЗИ брюшной полости отмечается положительная динамика в виде уменьшения размеров печени и селезенки. Девочка выписана домой 13.10.09 г. с рекомендациями: наблюдение гематолога, инфекциониста и педиатра, общий анализ крови с ретикулоцитами 1 раз в 3 месяца, контроль УЗИ брюшной полости.
Оба пациента находятся на диспансерном учете у врача-гематолога.
Диагноз врожденного микросфероцитоза представляет порой известные трудности. Наиболее типичные проявления гемолиза — желтушность склер и кожных покровов — не всегда бывают правильно расценены врачом. Описанные нами клинические случаи являются прямым подтверждением этого. У обоих пациентов с рождения определялись иктеричность склер и кожных покровов, но подробного обследования, до развития гемолитического криза, больным не проводилось. Наличие сходной симптоматики у отца девочки (синдром Жильбера?) дает возможность предположить, что пациентка Г. заболевание унаследовала от отца. Наследственность больного С. неизвестна.
В обоих случаях провоцирующим фактором развития гемолитического криза явился вирус Эпштейна — Барр. Дети и раньше болели вирусными инфекциями, но развития гемолитического криза они не вызывали. Возможно, не всякая, а лишь определенная группа вирусов может вызывать кризы. Этот вопрос остается открытым, так как на примере двух случаев нельзя утверждать, что вирус Эпштейна — Барр всегда провоцирует развитие гемолитического криза у больных наследственным микросфероцитозом.
Е.В. Ширданина, З.С. Гордеева
Йошкар-Олинская детская городская больница, г. Йошкар-Ола
Ширданина Екатерина Валерьевна — врач клинико-диагностической лаборатории
Литература:
1. Погорелов В.М., Козинец Г.И., Ковалева Л.Г. Лабораторно-клиническая диагностика анемий. — Москва. Медицинское информационное агентство, 2004. — C. 136-137.
2. Коколина В.Ф., Румянцев А.Г. Практическое руководство по детским болезням. Гематология/Онкология детского возраста. — Том 4. — М.: Медпрактика-М, 2004. — C. 169-172.
3. Воробьев А.И. Руководство по гематологии. — Том 2. — М.: Медицина, 1985. — C. 46-54.
4. Кишкун А.А. Руководство по лабораторным методам диагностики. М.: ГЭОТАР-Медиа, 2007. — C. 468-680.
5. Кассирский И.А., Алексеев Г.А. Клиническая гематология. — М.: Медицина, 1970. — C. 235-242.
6. Луговская С.А, Почтарь М.Е. Гематологический атлас. — М.: Триада, 2004. — 227 с.
7. Колоколов Г.Р., Герасина Е.В., Ананьев О.Л и др. Анализы. Полный справочник. — М.: Эксмо, 2008. — C. 497-499.
8. Максимов В.А., Дамидович К.К., Федорчук А.Н. и др. Редкие болезни, клинические синдромы и симптомы заболеваний органов пищеварения. — М.: АдамантЪ, 2007. — C. 128-129.
9. Рукавицин О.А., Скворцов С.В., Зенина М.Н. Гематология. Атлас-справочник. СПб: Детство-Пресс, 2009. — C. 219-220.
10. Погорелов В.М., Козинец Г.И., Дягилева О.А. и др. Цветной атлас клеток системы крови. — М.: Практическая медицина, 2007. — C. 98-99.
mfvt.ru
Микросфероцитарная гемолитическая анемия (болезнь Минковского - Шоффара). Медицинский портал Украины
Эта болезнь относится к наследственным заболеваниям, в основе которых лежит нарушение структуры белка в мембране эритроцита.
Распространенность
Наследственное заболевание
Наследственный микросфероцитоз (болезнь Минковского—Шоффара) широко распространен в странах Европы, реже встречается в Африке. На 1 млн населения приходится 200—300 случаев микросфероцитоза. Наследуется это заболевание по доминантному типу аутосомно, все больные являются гетерозиготными носителями гена болезни.
Этиология и патогенез
Более чем 100-летняя история изучения заболевания не позволила окончательно разрешить вопрос о природе сфероидального изменения эритроцитов и преждевременной их гибели. Однако в настоящее время считают, что сущность патологического процесса заключается в дефекте структуры мембраны эритроцитов. В 1968 году V. Weed и F. Bawdier предположили, что в основе наследственного сфероцитоза лежит генетически обусловленная аномалия мембранного белка — энзима. Несколько позже было показано, что при наследственном микросфероцитозе отсутствует белок мембраны эритроцитов — спектрин. Костный мозг при этом продуцирует неполноценные эритроциты, отличающиеся от нормальных тем, что они меньшего диаметра и имеют форму не двояковогнутой линзы, а двояковыпуклой, вследствие чего и названы микросфероцитами.
Наследственно измененные протеины клеточной мембраны обуславливают нарушение формирования нормальных контрактильных фибрилл. Это, в свою очередь, приводит к патологическому изменению формы эритроцита. Белок, подвергшийся мутационным изменениям, нарушает транспорт катионов, что способствует возникновению сфероцитоза, снижению осмотической резистентнjcnb, преждевременной гибели эрит- роцитов. Мембрана таких эритроцитов обладает повышенной проницаемостью для ионов натрия. Это приводит к их набуханию. Сферическая форма эритроцитов и особенности структуры белка их мембраны нарушают способность эритроцитов изменять свою форму в узкихместах кровотока, что приводит к их повреждению и разрушению. Основным местом гемолиза (гибели) является селезенка. Исследования показали, что продолжительность жизни эритроцитов у таких больных составляет 8—15 дней вместо 90—120 у здоровых людей.
Клинические проявления

Желтуха у новорожденных
Первые признаки заболевания могут проявиться и в детском возрасте, но чаще — в юношеском и зрелом. При заболевании микросфероцитозом отмечают желтуху, анемию, спленомегалию (увеличение селезенки), изменения скелета.
В течение длительного времени единственным признаком заболевания является желтушное окрашивание склер и кожи. Течение волнообразное. Причиной усиления гемолиза и, соответственно, ухудшения состояния чаще всего является инфекция, переохлаждение, беременность. Развивается слабость, появляется одышка и учащенное сердцебиение при физической нагрузке. Степень интенсивности желтухи может быть различной: от незначительной до резки выраженной. С каждым обострением желтушность усиливается. У детей первых месяцев жизни гипербилирубинемия бывает особенно высокой с резко выраженной желтухой и поражением ядер головного мозга (ядерная желтуха).
У детей старшего возраста проявление заболевания (кризов) нередко осложняется желчно-каменной болезнью, причем билирубиновые камни при рентгеноскопическом исследовании не обнаруживаются.
Характерным признаком заболевания является увеличение селезенки, а в дальнейшем — и печени. Селезенка может увеличиваться до значительных размеров. Увеличение ее обусловлено усиленным гемолизом в ней эритроцитов.
Анемия при микросфероцитозе зависит от степени гемолиза. В тяжелых случаях во время кризов, особенно у детей раннего возраста, уровень гемоглобина резко снижается (ниже 70 г/л), при этом характерны желтуха, бледность, одышка, тахикардия, сопровождаемые нередко тошнотой, рвотой, болями в животе, лихорадкой. У детей старшего возраста анемия может быть незначительной, или кризы протекают без анемиза- ции. Селезенка у этих больных, как правило, увеличена, плотная, безболезненная, от 1—2 см до 8—10 см ниже края реберной дуги. Нередко наблюдаются колебания в ее размерах: значительное увеличение при кризах и уменьшение в периоде относительного благополучия. У детей старшего возраста, перенесших много кризов, бывает увеличена печень. Значительно больших размеров достигает она и при тяжелом течении болезни у детей младшего возраста.
Скелет деформируется при раннем развитии заболевания. У такого ребенка через несколько лет хорошо определяются башенный череп, высокое (готическое) нёбо с нарушенным расположением зубов, укороченные мизинцы, деформация первого ребра, может быть косоглазие.
Диагностика
Диагностика заболевания
Для диагностики необходимы анализы крови. Распознавание заболевания основывается, прежде всего, на обнаруживании микросфероцитов — небольших размеров эритроцитов со средним диаметром менее 6,3 мкм, интенсивно окрашенных, без просветле- ния по центру. Средний диаметр нормальных эритроцитов составляет 7,2—7,5 мкм с центральным просветлением. Имеет значение увеличение количества ретикулоцитов, которое зависит от степени гемолиза. Во время гемолитических кризов число их возрастает очень значительно, в периферической крови могут появляться единичные нормоциты. Количество тромбоцитов всегдав норме. Число лейкоцитов в период кризов растет, нередко с нейтрофильным сдвигом, но чаще бывает в пределах нормы.
Лечение
При стабильном течении, когда заболевание проявляется слабо выраженной желтушной окраской кожи, при хорошем самочувствии и отсутствии анемии, каких-либо особых методов лечения не требуется.
Методом выбора при лечении наследственного микросфероцитоза является спленэктомия. Оптимальным возрастом для проведения этой операции, по мнению ряда авторов, следует считать 4—5 лет. Однако возраст пациента не должен рассматриваться как противопоказание к вмешательству. Тяжелые гемолитические кризы, непрерывное течение гемолитического криза, арегенераторные кризы — вот показания для проведения спленэктомии даже у детей раннего возраста. Причем наилучшие результаты получены у детей, оперированных в тот период болезни, когда еще не наступили выраженные нарушения со стороны печени, желчевыделительной системы, миокарда. Положительный эффект спленэктомии выявляется в первые дни после операции. Значительно умень- шаются желтушность и бледность кожных покровов, а к концу первой недели цвет кожи у большинства детей нормализуется. Быстро улучшается общее самочувствие детей. В первые часы после удаления селезенки значительно повышаются содержание гемоглобина и количество эритроцитов. У больных, оперированных на фоне выраженной анемии, восстановление эритропоэза и ликвидация анемии происходят лишь к концу первого месяца после вмешательства.
Берегите себя и будьте здоровы. Всегда с Вами ваш помощник в вопросах здоровья У ДОКТОРА.
Читайте также:
udoktora.net
Анемия минковского шоффара. Особенности лечения анемии Минковского-Шоффара (наследственного сфероцитоза)
Skip to main content- Личный кабинет
- Нейротехнологии.рф
- Главная
- Что это за сайт?
- Что такое нейротехнологии?
- Новости сайта
- Глоссарий терминов
- Команда
- Контакты и связь
- Статьи и публикации
- Все статьи
- Лечебная диета
- Причины заболеваний
- Свойства лекарств
- Поджелудочная железа
- Советы врачей
- Нейроновости
- Познавательные видео
- Мероприятия
- Документы
xn--c1adanacpmdicbu3a0c.xn--p1ai