Антифосфолипидный синдром: симптомы и лечение. Катастрофический антифосфолипидный синдром что это такое
виды, причины, симптомы и лечение
Антифосфолипидный синдром - основные симптомы:
Антифосфолипидный синдром – болезнь, включающая в себя целый симптомокомплекс, относящийся к нарушению фосфолипидного обмена. Суть патологии заключается в том, что человеческий организм принимает фосфолипиды за чужеродные тела, против которых вырабатывает специфические антитела.
Какой фактор является причиной формирования подобного недуга у женщин, мужчин и детей на сегодня остаётся неизвестным. Тем не менее клиницисты выделяют несколько предрасполагающих источников, среди которых инфекционные процессы вирусной или бактериальной природы.
Антифосфолипидному синдрому соответствует большое количество самых разнообразных проявлений, среди которых – повышение кровяного тонуса, поражение кожного покрова, формирование тромбов и пороков сердца.
Чтобы поставить правильный диагноз, необходим широкий спектр лабораторных исследований, которые в обязательном порядке должны дополняться инструментальными процедурами и тщательным обследованием клинициста.
Лечение патологии основывается на консервативных методиках, но при тяжёлом её протекании может понадобиться такая процедура, как плазмаферез.
В Международной классификации болезней подобному синдрому не выделено отдельного шифра, но он относится к категории «другие нарушения свёртываемости», отчего код по МКБ-10 будет – D 68.0.
Этиология
Причины, на фоне которых развиваются фосфолипидные синдромы остаются неизвестными, однако специалисты из области гематологии и ревматологии отмечают присутствие нескольких предрасполагающих факторов.
Таким образом, мужчины, женщины и дети подвергаются формированию подобного заболевания на фоне:
Крайне опасен антифосфолипидный синдром для беременных представительниц женского пола. Именно у такой категории пациентов наиболее часто наблюдается развитие осложнений не только с протеканием периода вынашивания ребёнка, но также с функционированием некоторых внутренних органов.
Точную степень встречаемости патологии установить не представляется возможным, однако известно, что в 4% случаев антифосфолипидным синдромам подвергаются совершенно здоровые люди. Примечательно то, что у представительниц женского пола антитела к фосфолипидам выявляются во время лабораторной диагностики в несколько раз чаще, нежели у мужчин. Более того, клиницистами установлено, что чем старше человек, тем чаще у него выявляется подобное отклонение, отчего у ребёнка оно развивается крайне редко.
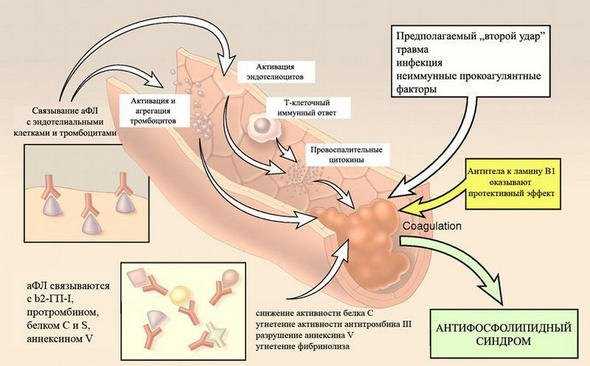
Патогенез антифосфолипидного синдрома
Классификация
Существует несколько основных разновидностей такой болезни:
- первичный антифосфолипидный синдром – характеризуется развитием при отсутствии протекания того или иного заболевания. Его причины остаются невыясненными, но считается, что влияет отягощённая наследственность, вялотекущие инфекции и передозировка лекарствами;
В зависимости от клинических проявлений выделяют такие особые формы болезни:
- катастрофический АФС – выражается в стремительном течении, развитии недостаточности всех систем и внутренних органов, что обуславливается формированием тромбов как больших, так и малых размеров;
- АФС в сочетании с васкулитом – в таких ситуациях наблюдается протекание воспалительных процессов в сосудах;
- синдром гипотромбинемии – при таком варианте протекания отмечается недостаточное количество тромбина в крови. Это вещество принимает участие в процессе её свёртываемости и образовании кровяного сгустка;
- микроангиопатические синдромы – в свою очередь, делятся на гемолитико-уремический синдром, тромботическую или тромбоцитопеническую пурпуру и HELLP-синдром;
- диссеминированное сосудистое свёртывание – помимо нарушения работы свёртывающей системы крови и появления тромбов, происходит развитие кровоизлияний.
Клинические критерии антифосфолипидного синдрома – это не основные факторы, составляющие классификацию патологии. Также существует группа лабораторных критериев, которая делит АФС на:
- серопозитивный – основные разновидности антител к фосфолипидам обнаруживаются у пациента путём осуществления широкого спектра лабораторных исследований крови;
- серонегативный – антитела не определяются в анализе крови больного.
Симптоматика
Антифосфолипидные синдромы состоят из большого количества самых разнообразных клинических проявлений, которые будут отличаться в зависимости от поражённого сегмента.
Самым первым и распространённым признаком болезни выступает формирование тромбов, которые могут быть венозными (встречаются в несколько раз чаще) и артериальными. Наиболее часто в патологию вовлекаются вены ног, печени, почек и сетчатки, а также церебральные артерии.
Тромбоз вен нижних конечностей имеет такие признаки:
- интенсивный болевой синдром;
- отёчность;
- покраснение кожных покровов поражённого сегмента;
- образование гангрен и язв на больной ноге.
Тромбы ног могут отсоединяться от стенок сосудов и с потоком крови достигать лёгочной артерии, что приводит к появлению:
При поражении почек и печени симптомы будут следующими:
- увеличение объёмов того или иного органа;
- скопление большого количества жидкости в брюшине, что также носит название асцит;
- изменение состава крови, а именно понижение концентрации калия и холестерина;
- признаки портальной гипертензии.
Если патология затрагивает ЦНС, то симптоматическая картина будет включать в себя:
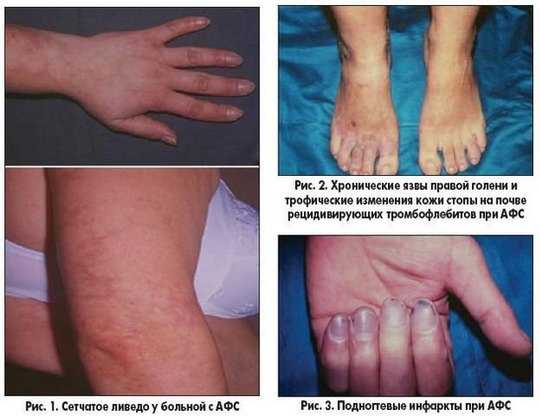
Клинические проявления антифосфолипидного синдрома
Помимо этого, в симптоматику АФС входят:
- кровоизлияния в ЖКТ;
- инфаркт селезёнки;
- кожная эритема с локализацией на ладонях и стопах;
- сетчатое ливедо;
- гангрена пальцев;
- появление трофических язв на кожном покрове;
- двигательная слабость;
- потеря зрения;
- общая амнезия;
- малокровие;
- нарушение ЧСС.
Весь вышеуказанный симптомокомплекс характерен как для взрослых, так и для детей, однако у последней категории пациентов патология протекает тяжелее.
Антифосфолипидный синдром у беременных представлен такими симптомами:
- отёчностью ног и покраснением кожи;
- образованием незаживающих язв;
- болезненностью в области груди;
- ощущением нехватки воздуха;
- головными болями;
- онемением конечностей;
- одышкой;
- временными нарушениями остроты зрения, координации и памяти;
- мраморной окраской кожи;
- самопроизвольным прерыванием беременности;
- преждевременной родовой деятельностью.
Кроме этого, велика вероятность отягощённого протекания периода вынашивания ребёнка, что заключается в развитии эклампсии или преэклампсии.
Диагностика
Благодаря тому, что заболевание имеет ярко выраженные клинические проявления, а также обладает специфическими лабораторными отклонениями, с установлением правильного диагноза не возникает проблем. Тем не менее для его уточнения требуются инструментальные обследования и осуществление ряда манипуляций, проводимых непосредственно гематологом.
Таким образом, первичные диагностические мероприятия включают в себя:
- изучение истории болезни не только пациента, но и его близких родственников – для выявления наиболее соответствующего тому или иному человеку предрасполагающего фактора;
- сбор и анализ жизненного анамнеза – сюда также стоит отнести информацию о протекании беременности;
- тщательный физикальный осмотр, включающий в себя пальпацию живота, осмотр конечностей, оценивание остроты зрения и состояния кожи, а также прослушивание пациента при помощи фонендоскопа и измерение кровяного тонуса;
- детальный опрос больного – для определения степени выраженности симптомов, что укажет на вариант протекания недуга.
В лабораторную диагностику входят:
- общеклинический анализ крови;
- коагулограмма – для оценивания свёртываемости крови;
- проба Кумбса;
- иммуноферментный анализ крови;
- серологические тесты;
- биохимия крови.
Инструментальная диагностика антифосфолипидного синдрома направлена на осуществление:
- доплерографии сосудов;
- УЗИ плода;
- ЭКГ и ЭхоКГ;
- кардиографии;
- рентгенографии брюшины;
- УЗДГ артерий и вен ног, сосудов почек, печени и головы.
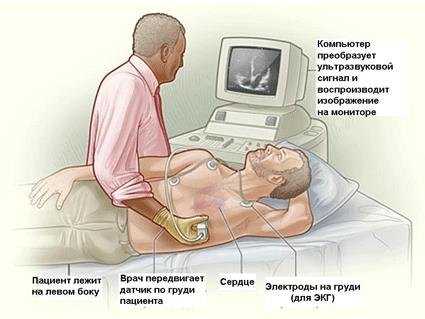
Проведение ЭхоКГ
В дополнение может понадобиться консультация и обследование у таких специалистов:
- гастроэнтеролог;
- кардиолог;
- акушер-гинеколог;
- нефролог;
- педиатр;
- нефролог;
- терапевт;
- ревматолог.
Лечение
Несмотря на то что клиническая картина АФС негативное влияние на многие внутренние органы и системы человеческого организма, терапия болезни заключается в том, чтобы использовать консервативные методики, которые также направлены на предупреждение развития осложнений.
Медикаментозное лечение включает в себя приём:
- прямых и непрямых антикоагулянтов;
- глюкокортикоидов – при катастрофическом АФС;
- антиагрегантов;
- антибактериальных средств.
В случаях тяжёлого протекания антифосфолипидного синдрома у мужчин, женщин и детей, показано:
- внутривенное введение иммуноглобулина;
- осуществление плазмафереза;
- переливание свежезамороженной плазмы.
Кроме этого, лечение должно включать в себя:
- осуществление умеренной физической активности;
- отказ от длительного нахождения в неподвижном состоянии и занятия активными видами спорта;
- избегание авиаперелётов;
- исключение применения пероральных контрацептивов.
Иные способы терапии, в частности народная медицина, при антифосфолипидном синдроме не используются.
Возможные осложнения
Несвоевременная диагностика антифосфолипидного синдрома, игнорирование клинических признаков и неадекватная терапия влечёт за собой формирование большого количества осложнений, среди которых:
Для беременных представительниц женского пола патология чревата:
- внутриутробной гибелью плода;
- выкидышами;
- преждевременными родами;
- неразвивающейся беременностью;
- гемолитической болезнью плода;
- внутриутробной гипоксией плода.
Профилактика и прогноз
На фоне того, что точные причины развития болезни остаются неизвестными, профилактические клинические рекомендации направлены на соблюдение общих правил:
- ведение здорового и в меру активного образа жизни;
- применение только тех медикаментов, которые выпишет клиницист;
- своевременное лечение бактериальных и вирусных инфекционных процессов, а также других недугов, которые могут вызвать появление АФС;
- регулярное посещение акушера-гинеколога – показано беременным женщинам.
Кроме этого, не стоит забывать про профилактические осмотры в медицинском учреждении и сдачу анализов крови не реже двух раз в год.
Прогноз, а также ответ на вопрос – можно ли вылечить антифосфолипидный синдром, будет индивидуальным для каждого больного. Первичный АФС, при условии ранней диагностики, обладает благоприятным исходом беременности и родовой деятельности. Прогноз вторичного варианта возникновения патологии диктуется базовой болезнью. Катастрофический АФС зачастую заканчивается летальным исходом.
Поделиться статьей:
Если Вы считаете, что у вас Антифосфолипидный синдром и характерные для этого заболевания симптомы, то вам могут помочь врачи: ревматолог, гематолог.
Также предлагаем воспользоваться нашим сервисом диагностики заболеваний онлайн, который на основе введенных симптомов подбирает вероятные заболевания.
Заболевания со схожими симптомами:
Стеноз сосудов – это термин в медицине, который характеризует сужение сосудов кровеносной системы. Он очень часто возникает вследствие развития атеросклероза в полости коронарных артерий. Образование этой патологии приводит к закрытию артерий, вследствие накопления бляшек, которые препятствуют току крови по телу. Опасность их образования и разрастания обусловлена тем, что они могут отрываться от стенок сосудов и двигаться по кровеносной системе, а попав в небольшой сосуд, полностью его закупорить.
... Ишемия (совпадающих симптомов: 6 из 20)Ишемия – патологическое состояние, которое возникает при резком ослаблении кровообращения в определённом участке органа, или же во всём органе. Патология развивается из-за уменьшения притока крови. Дефицит кровообращения становится причиной нарушения метаболизма, а также приводит к нарушению функционирования определённых органов. Стоит отметить, что все ткани и органы в человеческом теле имеют различную чувствительность к недостатку кровоснабжения. Менее восприимчивы — хрящевые и костные структуры. Более уязвимы – головной мозг, сердце.
...Кардиомиопатии – группа недугов, которых объединяет то, что во время их прогрессирования наблюдаются патологические изменения в структуре миокарда. Как следствие, эта сердечная мышца перестаёт полноценно функционировать. Обычно развитие патологии наблюдается на фоне различных внесердечных и сердечных нарушений. Это говорит о том, что факторов, которые могут послужить своеобразным «толчком» для прогрессирования патологии, довольно много. Кардиомиопатия может быть первичной и вторичной.
...Диабетическая полинейропатия проявляется как осложнение сахарного диабета. Основывается недуг на повреждении нервной системы больного. Зачастую недуг формируется у людей через 15–20 лет после того, как развился сахарный диабет. Частота прогрессирования недуга до осложнённой стадии составляет 40–60%. Заболевание может проявиться у людей как с 1 типом болезни, так и со 2.
...Узелковый периартериит – заболевание, которое поражает сосуды мелкого и среднего калибра. В официальной медицине заболевание именуется некротизирующий васкулит. Встречается название периартериит, болезнь Куссмауля-Майера, панартериит. По мере развития патологии образуются аневризмы, повторное поражение не только тканей, но и внутренних органов.
...simptomer.ru
Антифосфолипидный синдром
Изучение роли иммунопатологических процессов в патогенезе акушерских осложнений в последнее время позволило выделить симптомокомплекс, развивающийся в тех случаях, когда взаимоотношения матери и плода принимают характер аутоиммунных реакций.
Причем, аутоиммунная патология, выявляемая при беременности, в данном случае является частным случаем общего патологического процесса, характеризующегося образованием антител к фосфолипидам — универсальному компоненту клеточных мембран и митохондрий с последующими нарушениями в системе гемостаза и другими клиническими проявлениями.
Этот процесс носит название антифосфолипидного синдрома (АФС) и характеризуется рядом клинических проявлений:
1) развитием в молодом возрасте (до 45 лет) венозных или артериальных тромбозов, в частности, инфарктов, инсультов, преходящих нарушений мозгового кровообращения, тромбоэмболии легочной артерии, тромбозов сосудов сетчатки;
2) обнаружением волчаночного антикоагулянта (ВА) в венозной крови, как минимум двукратно с интервалом в 6—8 недель;
3) клинически выраженной или бессимптомной тромбоцитопенией;
4) акушерским анамнезом, осложненным потерей плода на разных сроках беременности (особенно в срок 10 нед. и более, когда маловероятна гибель плода вследствие генетических причин).
Патологическим процессом, на основе которого развиваются эти осложнения, является хронический ДВС-синдром.
Различают первичный АФС и вторичный — при наличии какого-либо аутоиммунного заболевания.
Существует несколько классификаций АФС:
D. С. Alarson-Segovia at al. (1995) выделяют следующие группы больных.
Больные с определенным АФС — при наличии двух и более клинических проявлений и повышенном уровне АКЛ-антител.
Больные с вероятным АФС имеют один клинический признак и высокий уровень АКЛ-антител или два клинических признака и умеренное увеличение антител к кардиолипину.
Сомнительный диагноз АФС можно поставить у больных с двумя и более клиническими симптомами при низких титрах AKЛ-антител или при отсутствии клинических проявлений на фоне высоких титров антител к кардиолипину.
По формам выделяют следующие варианты АФС (В. И. Кулаков с соавт., 2000):
1. АФС у больных с достоверным диагнозом СКВ или другим аутоиммунным заболеванием.
2. АФС у больных с волчаночноподобными проявлениями.
3. Первичный АФС.
4. Катастрофический АФС (острая диссеминированная коагулопатия с острым мультиорганным тромбозом).
5. Серонегативный АФС.
В зависимости от локализации тромбозов R.L.Bick, D.Ancypa (1995) различают четыре типа АФС:
I — тромбоз глубоких вен и тромбоэмболия легочных артерий;
II — тромбоз коронарных или периферических артерий;
III — тромбоз сосудов мозга и/или сетчатки глаза;
IV — смешанные тромбозы.
Наиболее опасной формой АФС является катастрофический антифосфолипидный синдром. Он развивается при воздействии провоцирующих факторов (инфекционные вмешательства или оперативные вмешательства) и проявляется быстро прогрессирующей полиорганной недостаточностью. На первый план в клинике заболевания может выступать острый респираторный дистресс-синдром, острая почечная или надпочечниковая недостаточность, нарушения мозгового или коронарного кровообращения, артериальные и венозные тромбозы. Быстро нарастает ступор, дезориентация. Без своевременного лечения смертность при этой форме заболевания составляет 60%.
Частота АФС в популяции, по данным американских авторов, составляет 5%; у пациенток с привычным невынашиванием в анамнезе распространенность АФС составляет 27—42% (В. И. Кулаков с соавт., 2000).
Наличие антифосфолипидных антител (АФА) можно предположить у следующих категорий больных:
- у больных с аутоиммунной патологией;
- у больных с артериальными и венозными тромбозами, церебро-васкулярными заболеваниями;
- при тромбоцитопении неясного генеза;
- у пациентов с ложно-положительной реакцией на сифилис;
- у женщин с привычным невынашиванием беременности неясного генеза;
- у женщин с внутриутробной гибелью плода во II и III триместрах беременности;
- у беременных с ранним развитием гестоза, при задержке внутриутробного развития плода.
Необходимо отметить также роль хламидийной инфекции, когда АФА перекрестно реагируют с липополисахаридом клеточной стенки хламидии, структурно схожей с фосфолипидами. В настоящее время хламидийная инфекция относится к факторам риска инфарктов, инсультов, развития атеросклероза.
Кроме того, синтез аутоантител может провоцироваться полисахаридными антигенами, содержащимися в капсулах бактерий и вирусными антигенами, что объясняет возникновение тромботических осложнений у больных с АФС при обострении вирусных инфекций.
Появление аутоантител (ВА и АКЛ-антител) связывают с генетически обусловленным несовершенством иммунной системы. Известна наследственная предрасположенность к аутоиммунным заболеваниям, в том числе — АФС.
Антитела к фосфолипидам могут образовываться под влиянием как экзо-, так и эндогенных факторов.
Экзогенные факторы, в основном инфекционные (сифилис, малярия, инфекционный мононуклеоз, туберкулез, гепатит А), вызывают образование транзиторных антител, не вызывающих тромбоэмболических осложнений. Кроме того, установлено, что такие «инфекционные» антитела реагируют непосредственно с отрицательно заряженными комплексами фосфолипидов оболочки микроорганизма вне зависимости от наличия кофакторов. Эта группа антител представлена в основном IgM и, в меньшей степени — IgG (IgG, и IgG3), определяется в сыворотке в низкой концентрации и не обладает антикоагулянтной активностью.
В отличие от этой группы антител, под влиянием эндогенных факторов образуются так называемые «аутоиммунные» антитела. Для их взаимодействия с аутоантигенами (например, фосфолипидами мембран тромбоцитов, эндотелиоцитов, кардиолипином и другими) необходимо наличие плазменного кофактора — β2- гликопротеина 1 (β2-ГП-1). Эти антитела обнаруживаются в сыворотке крови в высокой концентрации, представлены в большей степени IgG (IgG2 и IgG4) и меньшей — IgM. Они обладают антикоагулянтной активностью, с ними связано нарушение эндотелиального гемостаза с развитием тромбоэмболических нарушений (инсультов, инфарктов, тромбозов и тромбоэмболий).
Антитела к фосфолипидам — это гетерогенная группа антител, различающаяся по специфичности к определенному классу мембранных фосфолипидов.
Отдельная группа антител, называемая «волчаночным антикоагулянтом» (ВА), удлиняет in vitro фосфолипидзависимые коагуляционные реакции, воздействуя на Са++-зависимое связывание протромбина и фХа, фVа в процессе сборки протромбинактиваторного комплекса (протромбиназы). Эти антитела реагируют с фосфолипидами клеточных мембран (фосфатидилэтаноламином, фосфатидилхолином, фосфатидилсерином, фосфатидилинозитолом, фосфатидиловой кислотой).
Другая группа антител определяется как антикардиолипиновые антитела (АКЛ-антитела) — к компоненту внутренней мембраны митохондрий — кардиолипину.
Обнаружена возможность перекрестной реакции антифосфолипидных антител (АФА) к другим аутоантигенам — к ДНК, Fc-фрагменту Ig, мембране тромбоцита, эндотелиоцита, эритроцита.
Для выявления АФА используются несколько методов. Для определения ВА наиболее распространены функциональные тесты, основанные на подавлении in vitro сывороткой крови больных фосфолипидзависимых коагуляционных реакций без воздействия на активность факторов свертывания крови.
Лысенков С.П., Мясникова В.В., Пономарев В.В.
Неотложные состояния и анестезия в акушерстве. Клиническая патофизиология и фармакотерапия
medbe.ru
Антифосфолипидный синдром - лечение, причины, симптомы
 Антифосфолипидный синдром – это комплекс клинико-лабораторных нарушений, проявляющихся склонностью к повышенному тромбообразованию, тромбоцитопении и системными гематологическими нарушениями, обусловленными изменениями аутоиммунного характера.
Антифосфолипидный синдром – это комплекс клинико-лабораторных нарушений, проявляющихся склонностью к повышенному тромбообразованию, тромбоцитопении и системными гематологическими нарушениями, обусловленными изменениями аутоиммунного характера.
Основную категорию риска по антифосфолипидному синдрому составляют женщины в период беременности, и частота встречаемости симптомокомплекса в этой категории пациенток составляет не менее 5%. Достоверно установить статистические данные встречаемости данной патологии среди всего взрослого населения не представляется возможным, так как в некоторых случаях у абсолютно здорового человека могут наблюдаться пограничные показатели антифосфолипидных антител в циркулирующей крови.
При отсутствии своевременных лабораторно-диагностических и лечебных мероприятий создаются условия для значительного расстройства здоровья пациента и даже угрозы для жизни больного, поэтому лиц, относящихся к группе риска необходимо систематически обследовать на предмет наличия признаков антифосфолипидного синдрома.
Причины антифосфолипидного синдрома
Достоверных этиопатогенетических факторов, в 100% случаев провоцирующих развитие антифосфолипидного синдрома, не существует, однако существует четкая корреляция между появлением признаков данной патологии у лиц, страдающих заболеваниями ревматической и аутоиммунной природы. Кроме того, повышенный синтез антител к фосфолипидам наблюдается при большинстве заболеваний вирусной и бактериальной природы и имеющихся у пациента онкологических злокачественных патологий различной локализации.
В связи с тем, что последние научные исследования в области иммунологии доказали факт генетической предрасположенности к развитию аутоиммунных нарушений, антифосфолипидный синдром, в патогенезе которого существенную роль играют нарушения иммунного характера, можно отнести к категории заболеваний генетической природы.
Антифосфолипидные антитела представляют собой гетерогенную популяцию специфических антител, взаимодействующих с фосфолипидами, входящими в состав эндотелия сосудов и тромбоцитов, тем самым провоцируя активацию тромбоцитарных клеток, утрату антитромбогенных свойств сосудистого эндотелия и нарушение фибринолитических процессов.
Таким образом, основу патогенеза развития антифосфолипидного синдрома составляет персистирующая активация гемостатической системы обусловленная усилением протромботических процессов с одновременным ослаблением антитромботических процессов в организме, что неизбежно приводит к рецидиву тромбообразования.
Согласно патогенетической теории, признаки антифосфолипидного синдрома возникают в результате непосредственного усиления процессов гиперкоагуляции под воздействием циркулирующих антифосфолипидных антител («первый удар») с последующим воздействием локальных тригерных механизмов, как факторов индукции тромбообразования («второй удар»).
В ситуации, когда невозможно достоверно установить связь развития аутоиммунных нарушений с каким-либо этиологическим фактором, устанавливается заключение «первичный антифосфолипидный синдром».
Группа риска по данной нозологической форме представлена пациентами, длительно находящимися на постельном режиме в послеоперационном периоде, женщинами, длительно принимающими комплексные гормональные средства контрацепции, а также всеми лицами, имеющими признаки повышенного холестерина в крови.
Симптомы антифосфолипидного синдрома
Наиболее тяжелыми и одновременно самыми часто встречающимися клиническими проявлениями антифосфолипидного синдрома являются сосудистые тромбозы различной локализации и тяжелые формы акушерской патологии. Проявления тромбоза могут быть самыми различными в зависимости от распространенности патологического процесса и калибра пораженного сосуда. В международной хирургической практике существует мнение, что при антифосфолипидном синдроме развиваются множественные васкулопатии невоспалительной природы, сопровождающиеся окклюзией просвета сосуда.
Дебют тромботических проявлений антифосфолипидного синдрома, как правило, наблюдается при поражении глубоких вен дистальных отделов нижних конечностей, но в некоторых случаях могут наблюдаться и признаки поражения сосудов артериального русла (потеря всех видов чувствительности, похолодание кожных покровов, трофические изменения кожи и подкожной клетчатки). Излюбленной локализацией артериальных тромбозов при антифосфолипидном синдроме являются внутримозговые артерии, при возникновении которых развивается тяжелая общемозговая неврологическая симптоматика.
При поражении структур центральной нервной системы, обусловленном ишемическими нарушениями, наблюдаются различные степени неврологических проявлений от транзиторной ишемической атаки до развития стойких психоневрологических симптомов ишемического инсульта. При развитии типичного приступа транзиторной ишемической атаки, у пациента отмечается кратковременная утрата сознания с последующим головокружением, парестезии, нарушением зрительной функции и транзиторным типом амнезии. В случае рецидивирующего течения транзиторной ишемической атаки, создаются условия для развития деменции с выраженными когнитивными нарушениями. На этой стадии антифосфолипидного синдрома затруднительна постановка диагноза, так как клинические проявления могут симулировать сенильную форму деменции.
Самой частой жалобой пациентов, страдающих антифосфолипидным синдромом, являются частые эпизоды мигренозной головной боли, сопровождающиеся транзиторной потерей зрения.
Гиперпродукция антифосфолипидных антител способствует тромбированию сосудов различной локализации, в том числе и коронарных артерий, что одинаково часто встречается у лиц разной возрастной категории, в том числе и у детей. У лиц пожилого возраста данные изменения неизбежно приводят к развитию клинического симптомокомплекса инфаркта миокарда. Пациенты молодого возраста, имеющие лабораторные признаки антифосфолипидного синдрома, в большей степени подвержены появлению изменений клапанного аппарата сердца, проявляющиеся гемодинамическими нарушениями различной глубины.
В связи с тем, что тромботические проявления антифосфолипидного синдрома наблюдаются практически во всех органах человеческого организма, симптомами поражения почек является выраженная протеинурия и развитие клинической картины нефротического синдрома.
Тромбоз мелких капиллярных сосудов с локализацией в кожных покровах сопровождается появлением характерной геморрагической сыпи и трофических нарушений кожи.
Поражение органов желудочно-кишечного тракта заключается в повышенной склонности к желудочным кровотечениям и развитию клиники мезентериального тромбоза (острая боль в брюшной полости без четкой локализации, расстройства стула, неукротимая рвота, положительные симптомы раздражения брюшины).
Антифосфолипидный синдром при беременности
К сожалению, несвоевременная диагностика и отсутствие лечебных мероприятий, направленных на устранение признаков антифосфолипидного синдрома у беременной женщины может стать причиной тяжелых осложнений, как в период вынашивания плода, так и в момент родоразрешения. В некоторых ситуациях, заключение «антифосфолипидный синдром» устанавливается только лишь после нескольких эпизодов преждевременного прерывания беременности на разных сроках.
Существует статистика, согласно которой даже у абсолютно здоровой беременной женщины в 2% случаев наблюдаются транзиторные эпизоды повышения уровня антифосфолипидных антител, обусловленные иммунными нарушениями и требующими динамического лабораторного контроля без медикаментозной коррекции.
Клинические проявления и степень их проявления зависят не столько от лабораторного титра антифосфолипидных антител, сколько от срока беременности, в течение которой они появились. Так, в первом триместре беременности наличие антител к фосфолипидам может стать провокатором возникновения самопроизвольного аборта. Второй триместр беременности у женщины, страдающей антифосфолипидным синдромом, протекает с признаками внутриутробной задержки развития плода и эпизодами преэклампсии. Третий триместр опасен в отношении развития таких тяжелых осложнений, как внутриутробная гибель плода или преждевременно наступившие роды.
Все вышеперечисленные патологические состояния объясняются тромботическим влиянием антифосфолипидных антител на сосудистую плацентарную систему, обеспечивающую внутриутробное питание плода. Кроме того, антифосфолипидный синдром при беременности запускает каскад гормональных изменений в организме беременной женщины, имеющих большое значение в регуляции процесса внутриутробного развития плода.
Существует четкая зависимость между высоким уровнем антифосфолипидных антител в крови женщины репродуктивного возраста и невозможностью зачатия ребенка, обусловленной нарушением процесса имплантации бластоциста.
В связи с тем, что антифосфолипидный синдром относится к категории заболеваний, провоцирующих тяжелые акушерские патологии, его диагностика должна входить в состав алгоритма обязательного обследования женщин, страдающих бесплодием и привычным невынашиванием плода.
В случае лабораторно подтвержденного антифосфолипидного синдрома, всем пациенткам до наступления беременности рекомендовано применение препаратов глюкокортикоидного ряда в минимальной дозировке (Преднизолон в суточной дозе 5 мг) под постоянным контролем титра антител к фосфолипидам и показателей коагулограммы. В ситуации затяжного течения антифосфолипидного синдрома, беременная женщина вынуждена принимать кортикостероиды весь период беременности, и даже ранний послеродовый период. Длительную гормональную терапию следует проводить «под прикрытием» Иммуноглобулина в дозировке 25 мл курсом трое суток с целью предотвращения возможного рецидива острой вирусной инфекции.
Для того чтобы минимизировать побочные проявления применяемых с лечебной целью при антифосфолипидном синдроме лекарственных средств, рекомендовано проведение тщательного обследования и медикаментозной подготовки пациентки в период планирования беременности.
Минимальные диагностические мероприятия в течение беременности заключаются в проведении оценки степени развития плода по данным ультразвукового исследования с периодичностью не менее 1 раза в месяц, допплерометрии с целью исключения патологии плацентарного кровообращения и в третьем триместре регулярной кардиотокографии.
Лабораторный анализ на антифосфолипидный синдром впервые производится на шестой неделе беременности и непосредственно перед родами. Кроме того, пациенткам с антифосфолипидным синдромом должно систематически проводиться исследование показателей свертывающей системы, включая ранний послеродовый период, в котором имеется высокий риск возникновения тромбоэмболических осложнений.
При имеющихся изменениях коагулограммы, свидетельствующих в пользу активации процесса тромбообразования, всем беременным и родильницам рекомендовано продолжение антикоагулянтной терапии (Гепарин в суточной дозе 10 000 ЕД подкожно), которая является абсолютным противопоказанием для лактации.
Диагностика антифосфолипидного синдрома
В связи с тем, что антифосфолипидный синдром имеет самые различные клинические проявления, симулирующие другие патологии, для установления достоверного диагноза больному необходимо провести полное лабораторно-инструментальное обследование.
Специфическим лабораторным анализом при антифосфолипидном синдроме является исследование венозной крови на предмет наличия специфических маркеров, к которым относятся волчаночный антикоагулянт и антитела к кардиолипину. Данный анализ не обладает стопроцентной достоверностью и даже у здорового человека может наблюдаться ложноположительный результат, поэтому для подтверждения диагноза необходимо произведение трехкратного анализа с периодичностью три месяца.
Кроме того, неспецифические анализы в виде коагулограммы и развернутого анализа крови с подсчетом тромбоцитов, позволяют оценить степень тяжести антифосфолипидного синдрома, а также осуществлять контроль над проводимыми лечебными мероприятиями.
Инструментальные методы диагностики (магнитно-резонансная томография, компьютерная томография, эхокардиоскопия) позволяют оценить наличие тромботических изменений в сосудах, а также ишемические изменения в органах.
Для облегчения процесса установления диагноза «антифосфолипидный синдром», установлена единая система критериев постановки диагноза, включающая клинические и лабораторные критерии антифосфолипидного синдрома. В ситуации, когда у пациента наблюдается хотя бы один из клинических критериев в сочетании с лабораторным показателем, установление диагноза считается обоснованным.
Главным клиническим критерием данной патологии считается однократный или рецидивирующий эпизод тромбоза с различной протяженностью и локализацией. К акушерским клиническим признакам антифосфолипидного синдрома следует отнести: однократный или многократный самопроизвольный выкидыш, при котором плод не имеет аномалий развития, частые приступы преэклампсии и эпизоды преждевременно наступивших родов, замирание плода при условии отсутствия хромосомных аномалий у родителей.
Абсолютными лабораторными критериями является наличие высокого титра антикардиолипиновых антител группы М, увеличенная концентрация антител к бета-гликопротеину и волчаночному антикоагулянту дважды в течение трех месяцев.
Лечение антифосфолипидного синдрома
Несмотря на тенденцию к увеличению частоты встречаемости патологий, связанных с антифосфолипидным синдромом, до сих пор не разработаны единые международные стандарты наблюдения и лечения пациентов, страдающей той или иной формой синдрома. Однако после проведения многочисленных исследований с привлечением большой группы пациентов, удалось провести ретроспективный анализ варианта возможного исхода заболевания после применения того или иного метода лечения.
Существует множество вариантов комбинированной терапии антифосфолипидного синдрома, однако наибольшую эффективность в отношении коррекции аутоиммунных нарушений оказывают следующие комбинации препаратов: антикоагулянты прямого действия и глюкокортикостероиды, ацетилсалициловая кислота в сочетании с кортикостероидами, изолированный прием ацетилсалициловой кислоты, а также внутривенное введение иммуноглобулинов в максимальной дозировке.
При использовании кортикостероидной терапии рекомендовано применение пролонгированных форм препаратов в минимальной дозировке, во избежание возможных побочных реакций со стороны органов пищеварительного тракта.
Согласно рандомизированным исследованиям, комбинация минимальных доз Гепарина (10000 МЕ подкожно в сутки) с Ацетилсалициловой кислотой в суточной дозировке 75 мг имеет лучший эффект по сравнению с антиагрегантной монотерапией. В ситуации, когда у беременной женщины помимо лабораторных изменений, характерных для антифосфолипидного синдрома, наблюдался хотя бы один эпизод преэклампсии, целесообразно дополнить антикоагулянтную терапию Иммуноглобулином в суточной дозе 400 мг на 1 кг веса пациентки.
С целью устранения микроциркуляторных и сосудисто-тромбоцитарных нарушений рекомендовано применение Дипиридамола в суточной дозировке 150 мг, который можно использовать и при ранних сроках беременности.
При проведении активной антикоагулянтной терапии следует отдавать предпочтение низкомолекулярным гепаринам (Эноксипарин в суточной дозе 20 мг), которые можно использовать длительный период времени, не опасаясь развития побочных реакций в виде остеопороза и гепарининдуцированной тромбоцитопении. Областью их преимущественного применения считаются случаи антифосфолипидного синдрома у беременных женщин, так как действующее вещество не проникает через плаценту и не оказывает пагубного влияния на плод.
Доказанной эффективностью в отношении коррекции тромботических нарушений и устранения аутоиммунных нарушений обладает плазмаферез. Данная методика обладает дезинтоксикационными и иммунокоррегирующими свойствами, а также способностью значительно улучшать реологические показатели крови.
Критериями абсолютных показаний к применению лечебного плазмафереза у пациентов с антифосфолипидным синдромом являются: наличие высокой активности аутоиммунного процесса, некоррегируемая гиперкоагуляция, имеющиеся противопоказания к применению препаратов антикоагулянтной терапии, наличие побочных реакций от применения кортикостероидов.
Техника выполнения лечебного плазмафереза заключается в эксфузии 900 мл циркулирующей крови и замещение ее коллоидными растворами (10% раствор Альбумина).
В связи с тем, что антифосфолипидный синдром рано или поздно затрагивает коронарные артерии и способствует развитию тромбоза в системе коронарных артерий, многие исследователи пришли к выводу, что основную терапию данного состояния следует дополнять препаратами группы статинов (Аторвастатин 1 таблетка в сутки пожизненно).
Хирургические методы устранения признаков антифосфолипидного синдрома применяются только в случае тяжелого течения тромбоза сосудов после предварительной антикоагулянтной подготовки пациента.
vlanamed.com
Глава 1. : "Антифосфолипидный синдром"
 Книга: «Редкие неврологические синдромы и болезни» (В.В. Пономарев)
Книга: «Редкие неврологические синдромы и болезни» (В.В. Пономарев)
Антифосфолипидный синдром (АФЛС), еще недавно относившийся к разряду неврологических раритетов, в последние годы привлек к себе внимание ученых различных специальностей в связи с необычайным полиморфизмом клинических проявлений, мультисистемным поражением и длительным персистирующим течением. Впервые был описан G. R. Hughes и соавт. в 1986 г. при системной красной волчанке. Авторами было показано, что наличие в крови больных волчаночных антикоагулянтов и антикардиолипиновых антител (AKJI) ведет к развитию своеобразного симптомокомплекса, проявляющегося клинически артериальным и венозным тромбозом, гемолитической анемией, тромбоцитопенией, неврологической и акушерской патологией. Нередко при синдроме наблюдается поражение кожи в форме ливедо, возникают ливедоидные васкулиты, эндокардит, гипо- или гипертензия, синдром Рейно и гангрена пальцев [1, 10, 14]. Первоначально синдром был назван антикардиолипиновым, а затем АФЛС. В настоящее время выделяют первичный и вторичный АФЛС [10, 14, 16].
Возникновение вторичного АФЛС связывают с аутоиммунными, инфекционными, онкологическими заболеваниями и воздействием ряда лекарственных и токсических веществ [16]. Ряд авторов описывают так называемый катастрофический АФЛС, проявляющийся внезапным возникновением полиорганной недостаточности в ответ на оперативное вмешательство или острое инфекционное заболевание. Клинически он протекает в форме острого респираторного дистресс-синдрома, нарушения коронарного и мозгового кровообращения, дезориентации или ступора, острой почечной и надпочечниковой недостаточности с множественными тромбозами [10, 15]. У женщин АФЛС встречается в 2—5 раза чаще, чем у мужчин, при вторичном АФЛС это соотношение еще больше (7:1). В литературе описаны семейные случаи заболевания [2, 9]. Летальность при различных формах АФЛС колеблется от 17 до 60% [21, 27].
Основными диагностическими критериями АФЛС являются:
• наличие в венозной крови больного волчаночного антико-агулянта, выявляемого как минимум двукратно с интервалом в 6—8 недель;• возникновение в молодом возрасте артериальных и венозных тромбозов, инфаркта миокарда, инсультов, ТИА;• тромбоцитопения, проявляющаяся клинически или протекающая бессимптомно;• выкидыши у женщин, возникающие в сроки свыше 10 недель.
К дополнительным диагностическим критериям относят:
• сетчатое ливедо;• мигрень;• хорею;• эндокардит;• хронические язвы голеней.
Диагноз АФЛС можно поставить при сочетании одного из основных клинических и одного серологического признаков или при наличии двух и более дополнительных клинических признаков в сочетании с серологическими [1, 11, 17, 28].Приводим наблюдение с характерными для АФЛС неврологическими проявлениями.
Больная С., 27 лет, инженер. Поступила с жалобами на насильственное движение в мышцах лица, туловище, конечностях, затруднение речи, отечность правой голени. В детстве часто болела простудными заболеваниями. С 12-летнего возраста страдала классическими приступами мигрени. Приступы протекали однотипно с мерцанием «звездочек» и «мушек» перед глазами с последующей головной болью, чаще справа, и иногда заканчивались рвотой. К 25 годам приступы стали реже, повторяясь 2—3 раза в год. В 24 года перенесла генитальный герпес, подтвержденный вирусологически (в крови были обнаружены антигены вируса простого герпеса I и II типа). Был проведен курс лечения ацикловиром с иммунокорректорами. В 25 лет без видимой причины впервые развился флеботромбоз глубоких вен правой голени. В октябре 1999 г. возникли боли в грудной клетке, одышка, субфебрилитет. Лечилась в пульмонологическом, а затем в отделении сосудистой хирургии по поводу флеботромбоза правой подколенной вены, осложнившегося тромбоэмболией ветвей легочной артерии и инфаркт-пневмонией. В сентябре и октябре 2000 г. трижды повторялись кратковременные (по 15-30 мин) эпизоды расстройства речи, онемения и слабости в правых конечностях. При КТ головного мозга выявлено небольшое расширение левой сильвиевой щели.
Спустя год в отделении коллагенозов впервые был выставлен диагноз: АФЛС с высокой иммунологической активностью. В крови уровень АКЛ в 7 раз превышал показатель нормы (антитела получены в титре > 2,5 ед. при норме 0,35-0,40 ед.). После назначения курса лечения медролом и фенилином состояние улучшилось, продолжала работать. Через 6 месяцев появились насильственные движения в левой ноге, распространившиеся в последующие 1,5 месяца на всю левую половину туловища, включая лицо. В марте проходит лечение в неврологическом отделении областной больницы с диагнозом: хронический подкорковый энцефалит на фоне генерализованной герпетической инфекции с умеренным гиперкинетическим синдромом. Вторичный АФЛС вирусной этиологии. Тромбоз глубоких вен левой голени. Лечение циклодолом, фраксипарином, антигипоксантами, медролом эффекта не дало. В связи с нарастающим гиперкинезом направлена на госпитализацию. В семье подобными заболеваниями никто не болел. Замужем. Беременностей не было.
Объективно при поступлении: общее состояние удовлетворительное. Левая голень отечна. На конечностях мелкие подкожные гематомы. Тоны сердца ритмичные. Пульс 80 уд/мин, АД 130/80 мм рт. ст. Неврологический статус: эйфорична, эмоционально лабильна, астенизирована. Речь невнятная из-за оромандибулярного гиперкинеза. Недостаточность VII и XII пар черепных нервов слева по центральному типу. Хоботковый рефлекс. Парезов конечностей нет. Выраженная гипотония в левых
конечностях. Сухожильные и периостальные рефлексы средней живости без четкой разницы сторон. Брюшные и подошвенные рефлексы снижены S
Постоянные высокоамплитудные размахивания левыми конечностями. Кисти постоянно в движении с круговым разворотом в лучезапястном суставе. При эмоциях гиперкинез резко увеличивается. Вместе с тем пяточно-коленную и пальце-носовую пробу выполняет четко. В позе Ромберга устойчива. Походка резко нарушена из-за насильственных движений в левых конечностях.
Обследование: в анализе крови: НЬ — 125 г/л. Тромбоциты 296-109. ЛейкЬциты 8,2-109 (эозинофилы 10%), СОЭ 16 мм/ч. Анализ мочи в норме. СМЖ: белок 0,24 г/л, цитоз 3 • 106 клеток/л. Повторные исследования крови и ликвора на вирус простого герпеса дали отрицательный результат. Поданным иммунограммы отмечено незначительное снижение активности клеточного иммунитета (Т-активные лимфоциты 16%, норма 24—30%). УЗИ сердца: признаки уплотнения створок митрального клапана с митральной недостаточностью, регургитацией III степени. Глазное дно не изменено. При УЗИ брахиоцефальных артерий гемодинамически значимых нарушений кровотока в экстра- и интракраниальных отделах не выявлено. LE-клетки при многократных исследованиях не обнаружены. Реакция Вассермана в крови резко положительная. По данным коагулограммы: ПТИ — 103%, время рекальцификации АПТВ 49,2″, количество фибрина 4,2 г/л, время свертываемости по Ли-Уайту 8′, фибриноген В отрицательный, гематокрит 46/54. При МРТ головного мозга в кортикальной зоне левой теменной области обнаружены два мелких очага 6×6 мм и 3×3 мм, гиперинтенсивные в T2W режиме, расширение сильвиевой щели слева (рис. 5).
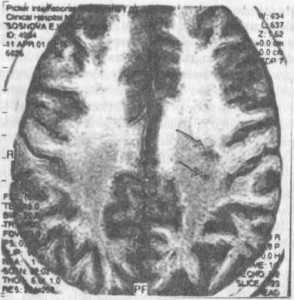
Рис. 5. МРТ головного мозга в T2w режиме больной С., 27 лет, с диагнозом АФЛС: в кортикальной зоне левой теменной области два мелких очага 6 и 3 мм в диаметре (указаны стрелками)
Приведенное наблюдение является яркой иллюстрацией АФЛС с трансформацией ряда характерных для него неврологических синдромов на этапах развития болезни. Возникновение у молодой женщины, страдающей мигренью, флеботромбоза глубоких вен голени, осложнившегося тромбоэмболией ветвей легочной артерии, нарушением мозгового кровообращения, хореей, в сочетании с высоким титром АКЛ и ложноположительной реакцией Вассермана делают диагноз АФЛС достоверным.Неврологические нарушения наряду с акушерской патологией — ведущие клиниче ские проявления АФЛС. Генез большинства неврологических нарушений связывают с гиперкоагуляцией и развитием тромбозов при данной патологии. Недавними исследованиями доказана способность антифосфолипидных антител вступать в соединение с фосфолипидозависимыми коагуляционными реакциями: с фосфолипидами мембран эндотелия сосудов, с мембранами тромбоцитов, эритроцитов [12, 21]. Возникающая при этом гиперкоагуляция идет за счет уменьшения выработки простациклина, снижения активации естественного антикоагулянта протеина С, угнетения фибринолиза, ингибирования антитромбина III, связывания В-гликопротеина I и изменения функции тромбоцитов [21, 23, 26].
Наиболее частое проявление АФЛС — нарушения мозгового кровообращения (НМК) [2, 6, 25]. Частота инфарктов мозга, вызванных тромбозом или эмболией интракраниальных сосудов, при АФЛС, по данным различных авторов, колеблется от 24 до 46% всех цереброваскулярных заболеваний [7, 8]. Средний возраст больных с НМК при АФЛС — 32-43 года, хотя, по мнению J. Pope и соавт., возраст начала заболевания может колебаться от 10 до 86 лет [22]. НМК могут протекать как в форме мозгового инсульта, так и в виде транзиторных ишемических атак (ТИА), как в нашем наблюдении. На долю ТИА приходится от 12 до 52% [5, 8]. Случаи внутримозговых кровоизлияний при АФЛС крайне редки [20]. Наблюдаемая последовательность развития ТИА после флеботромбоза глубоких вен голеней (реже — печеночных, подключичных и других вен) довольно частая. По данным Л. А. Калашниковой, такая закономерность достигает 26% [2]. Нередко НМК сочетаются с приступами мигрени. С другой стороны, мигрень длительное время может быть единственным самостоятельным неврологическим синдромом при АФЛС, как в нашем наблюдении. Генез мигренозных пароксизмов при АФЛС не до конца ясен, его связывают с взаимодействием АКЛ с фосфолипидами мембран тромбоцитов или самих нейронов [3, 18]. НМК может быть связано не только с тромбозом экстра- и интракраниальных сосудов, но и с часто встречающимся при АФЛС поражением сердца в форме уплотнения створок митрального клапана и нарушения регургитации различной степени. Не исключено, что именно кардиогенные микроэмболии из пораженных клапанов сердца были причиной ТИА у нашей больной.
Еще одно частое неврологическое проявление АФЛС — эпилептические припадки. Л. А. Калашниковой с соавт. отмечены четкие различия в характере эпилептических припадков при АФЛС и при постинсультной эпилепсии [4]. Эти отличия касаются в первую очередь структуры эпилептических приступов (генерализованные и комплексные при АФЛС и простые парциальные, часто с вторичной генерализацией при постинсультной эпилепсии), их выявленной взаимосвязи с перенесенным инсультом, локализации и размеров инфарктных очагов. По мнению авторов, в генезе эпилепсии при АФЛС ведущую роль играет опосредованное иммунологическое повреждение фосфолипидов мембран нейронов коры височной доли мозга и, как следствие, появление повышенной эпилептологической активности данных нейронов. Определенное значение, по-видимому, имеют и физиологические особенности кровоснабжения медиобазальных отделов височной доли мозга (стык двух артериальных бассейнов) [4, 9].
Хорея относится к числу дополнительных диагностических критериев при АФЛС. Гиперкинез при АФЛС может быть определенное время локальным, захватывая ту или иную конечность. Однако по мере прогрессирования процесса непроизвольные движения, как правило, генерализуются, ограничиваясь одной половиной тела или захватывая все конечности и мышцы лица. Гемихорею, первоначально возникшую у нашей больной, мы склонны были связать с НМК. Однако темп развития гиперкинеза, его регресс под влиянием плазмафереза и назначения малых доз галоперидола, данные МРТ головного мозга позволили отказаться от этого предположения. Большинство авторов считают, что в генезе хореи лежит аутоиммунно опосредованная дисфункция мозга, в частности дофаминовых структур в полосатом теле [4, 6].
К числу редких неврологических нарушений при АФЛС относятся миелопатия, синдром Гийена-Барре и другие невропатии [13, 19, 24]. В рамках АФЛС описан синдром Снеддона, при котором церебральные нарушения сочетаются с ливедо.Изменения при КТ и МРТ при АФЛС неспецифичны. Чаще они отражают наличие инфарктных очагов в веществе мозга и признаки атрофического процесса, нередко локально в зоне сильвиевой щели.
В лечении АФЛС выделяют два основных направления — патогенетическое и симптоматическое. Поскольку АФЛС — аутоиммунно опосредованная коагулопатия, то в клинике используют два принципиальных подхода к лечению и профилактике ее осложнений: воздействие на гемореологические показатели крови (антиагреганты и антикоагулянты) и снижение уровня активности АФЛС (кортикостероиды, иммуносупрессанты, внутривенные иммуноглобулины, плазмаферез). Четко отработанных схем лечения этими препаратами нет. Дозы подбираются индивидуально.
Таким образом, АФЛС проявляется полиорганными нарушениями, в том числе разнообразным поражением ЦНС и ПНС. В развитии заболевания основную роль играет аутоиммунная коагулопатия. В связи с междисциплинарным характером клинических проявлений такие больные наблюдаются врачами различных специальностей: неврологами, ревматологами, терапевтами, акушерами-гинекологами. Своевременная диагностика и комплексная терапия позволяют стабилизировать патологический процесс и в ряде случаев добиться стойкой ремиссии.
neyro-ro.ru
Антифосфолипидный синдром > Клинические рекомендации РФ (Россия) > MedElement
Рекомендации по ведению больных АФС с тромбозом1. Ведение пациентов с артериальными и/или венозными тромбозами и аФЛ, не набирающих критерий для достоверного АФС (серологические маркёры в низких уровнях), не отличается от ведения аФЛ негативных больных с подобными тромботическими исходами (уровень доказательства 1С)Комментарии. Данные системного обзора свидетельствуют, что пациенты с венозным тромбоэмболизмом и аФЛ, даже если они не набирают лабораторные критерии для диагноза АФС, лечение антикоагулянтами не отличается от ведения больных с тромбозами, не связанными с аФЛ [7,8]. Обычно вначале назначаются гепарины: нефракционированный (обычный), или низко-молекулярные , или пентасахариды, с последующим переводом на приём антагонистов витамина К (АВК) (варфарин).
2. Рекомендовано больным с определённым АФС и первым венозным тромбозом назначение антагонистов витамина К (АВК) с целевым значением международного нормализованного отношения (МНО) в пределах 2,0-3,0 (уровень доказательства 1В)Комментарии. В двух клинических исследованиях [9,10] было показано, что высоко-интенсивный уровень (МНО>3,0) гипокоагуляции не превосходит стандартный уровень (МНО 2,0-3,0) в профилактике рецидива тромбоза и ассоциировался с более частыми геморрагическими осложнениями. В одной из работ [11] по сравнению двух режимов высоко-интенсивного и стандартного, было показано что высокая интенсивность гипокоагуляции ассоциировалась с высокой частотой кровотечений, но и парадоксально с более частыми тромбоэмболическими осложнениями, что видимо, связано с частой флюктуацией МНО.
3. Пациенты с определённым АФС и артериальными тромбозами должны получать варфарин с целевым значением МНО > 3,0 или комбинировать с низкими дозами аспирина (МНО 2,0-3,0). (Уровень доказательства не градуирован в связи с отсутствием согласия.) Некоторые члены комиссии полагают, что только антиагреганты (аспирин или клопидогрель) или АВК с целевым МНО 2,0-3,0 будут одинаково обоснованы в этих ситуациях)Комментарии. В ретроспективном исследовании [12] было отмечено, что ни аспирин в низких дозах, ни антагонисты витамина К с достижением стандартной (средне-интенсивной степени) гипокоагуляции не были эффективны для вторичной тромбопрофилактики у больных с аФЛ и артериальными тромбозами. Другое проспективное двухгодичное исследование [13] не отметило различий в ответе ни на аспирин, ни на антикоагулянты у больных с инсультами аФЛ позитивных и негативных. Однако это исследование не может быть экстраполировано на популяцию больных с инсультами и достоверным АФС, уровни аФЛ были исследованы вначале включения в исследование, что могло привести к включению пациентов с транзиторно позитивными аФЛ. Различия в интенсивности гипокоагуляции обсуждаются последние 10 лет. В системном обзоре [7] было сделано заключение: для достоверного АФС высокий риск рецидива отмечался при стандартной гипокоагуляции, рецидив тромбоза был реже при МНО > 3,0. Сверх того, смерть из-за кровотечений была намного реже, чем смерть из-за тромбоза [7].
4. Оценка риска кровотечения у больного должна быть выполнена до назначения высокой степени гипокоагуляции или комбинирования антикоагулянтов и антиагрегантов (Уровень доказательства не градуирован)
5. Пациенты без СКВ с одним эпизодом инсульта, не связанного с кардиоэмболическим механизмом, с профилем аФЛ низкого риска тромбоза и наличием обратимых провоцирующих факторов могут отдельно считаться кандидатами для назначения антитромбоцитарных препаратов (Уровень доказательства не градуирован)
6. Больные с достоверным АФС и тромбозами должны длительно (пожизненно) получать антитромботическую терапию (уровень доказательства 1С)
7. Больным с одним случаем венозного тромбоза с профилем аФЛ низкого риска и известными преходящими преципитирующими факторами антикоагулянтная терапия может быть лимитирована в пределах 3-6 месяцев (Уровень доказательства не градуирован)
8. Пациентам с аФЛ, но без СКВ и без предшествующих тромбозов при профиле аФЛ высокого риска рекомендована долгосрочный приём низких доз аспирина, особенно при наличии других факторов риска тромбоза (уровень доказательства 2С)Комментарии. Первичная профилактика тромбоза должна проводиться у больных СКВ с аФЛ или с классическими кардиоваскулярными факторами риска, хотя эффективность аспирина в этих случаях оспаривается, преимущественно у больных без СКВ [14,15,16,17,18]
9. Больным СКВ с положительным ВА или стойко позитивными аКЛ в средних или высоких уровнях рекомендуется первичная тромбопрофилактика гидроксихлорохином (ГХ) (уровень доказательства 1В, некоторыми членами специальной комиссиb поддержан уровень доказательности 2В для использования ГХ) и низкие дозы аспирина (уровень доказательства 2В)Комментарии. ГХ кроме противовоспалительного действия , обладает антитромботическим эффектом ингибируя агрегацию тромбоцитов и высвобождение арахидоновой кислоты из активированных тромбоцитов [18].
10. Всем носителям аФЛ рекомендована тромбопрофилактика в ситуациях высокого риска тромбоза, таких как хирургические вмешательства, длительная иммобилизация и послеродовый период (уровень доказательства 1С) 11. У всех больных с профилем аФЛ высокого риска следует контролировать кардиоваскулярные факторы независимо от наличия предшествующих тромбозов, сопутствующей СКВ, или дополнительных АФС проявлений (уровень доказательства не градуирован) Комментарии. Больные АФС часто имеют другие дополнительные кардиоваскулярные факторы риска такие как: гипертензия, курение, гиперхолестеринемия, приём оральных контрацептивов [19,20,22,23].В исследовании случай-контроль [24] риск инсульта удваивался у курящих женщин с ВА, по сравнению с некурящими; использование контрацептивов увеличивало риск развития инсультов в 7 раз. В этом исследовании все женщины с инфарктом миокарда были курящими во время его развития.
Клинические рекомендации при акушерской патологии АФС Акушерская патология одна из крупных аспектов АФС и является критериальным признаком диагностических критерий АФС [1,2,3,25]. Акушерская патология АФС включает материнские тромбозы, рецидивирующие спонтанные аборты до 10 недель гестации, поздние нежелательные исходы беременности (например: внутриутробная гибель плода, преэклампсия, плацентарная недостаточность, задеожка внутриутробного развития плода, преждевременные роды). Даже при проведении оптимальной терапии согласно существующим рекомендациям неблагоприятные исходы у женщин с АФС до сих пор варьируют в пределах 20-30% случаев [27,28].
1. Тромбопрофилактика у бессимптомных аФЛ-позитивных женщин при ведении беременности и послеродовом периоде следует проводить согласно риск-стратифицированного подхода. (уровень доказательства не градуирован)
2. Гидроксихлорохин рекомендуется для первичной тромбопрофилактики у беременных бессимптомных аФЛ-позитивных женщин, особенно на фоне заболеваний соединительной ткани (уровень доказательства не градуирован) (уровень доказательства не градуирован) [29].
3. При возникновении ситуаций высокого риска тромбоза (периоперативный период, длительная иммобилизация) рекомендуются профилактические дозы гепарина для бессимптомных аФЛ-позитивных женщин [30]Комментарии. Необходимость тромбопрофилактики у женщин с аФЛ при отсутствии тромботических осложнений в анамнезе остаётся спорной среди экспертов. Прекращение курения и снижение индекса массы тела при его высоком уровне является одним из важных условий профилактики тромбоза у этих женщин [3]. Мнение экспертов было единогласным о высоком риске тромбоза в этой группе при приёме оральных контрацептивов. Некоторыми экспертами предложено сочетание их приёма с антикоагулянтами, но протромботический риск может перевешивать положительные моменты контрациптивов. Учитывая риск нежелательных явлений антикоагулянтов, большинство экспертов не согласны с продолжением приёма варфарина в послеродовом периоде у аФЛ-позитивных, но без клинических проявлений больных. В отношении приёма низких доз аспирина также мнение экспертов противоречиво. Это основано на заключениях двух рандомизированных исследований, где одно отметило успешное завершение беременности в этой группе женщин на фоне низких доз аспирина [31], второе – отметило неэффективность его в тромбопрофилактике [32]. Однако большинство работ подтверждают при аФЛ профиле высокого риска тромбоза профилактические дозы гепарина показаны.
4. Гепарины (нефракционированный или низко молекулярные) с или без низких доз аспирина рекомендуется для ведения беременных женщин с АФС (уровень доказательства 1с). Одобрено рекомендацией EULAR при ведении беременных женщин с СКВ и АФС [33]. Эффективность гепарина у женщин с АФС является доказанной и этому уделено большое внимание в литературе, на самом деле, в настоящее время отмечается его назначение беременным женщинам, у которых причина потери предыдущей неизвестна [34,35] . Кохрановский системный обзор и мета-анализ позволили сделать заключение, что применение нефракционного гепарина и аспирина снижало частоту потерь беременности до 54% у женщин с аФЛ и предыдущей акушерской патологией [36]. Информации о преимуществе низко молекулярных гепаринов над нефракционном гепарином в сочетании с аспирином недостаточно. В двух малых исследованиях была показана схожесть обоих гепаринов у беременных с аФЛ [37,38].
5. Вторичная профилактика тромбоза у женщин с АФС в послеродовом периоде пожизненная, с назначением антагонистов витамина К и поддержанием уровня гипокоагуляции от 2,0 до 3,0 - при венозных тромбозах и выше 3,0 – при артериальных . (уровень доказательства 1В)
6. Катастрофическая микроангиопатия во время беременности или в послеродовом периоде обычно включает эффективную антикоагулянтную терапию и в/в введение глюкокртикоидов (ГК) ± плазмаферез с последующим введением одногруппной свежезамороженной плазмы и в/в введение человеческого иммуноглобулина в зависимости от клинической ситуации.
В послеродовом периоде при резистентных формах имеются единичные сообщения об эффективности генно-инжинерной терапии (ритуксимаб, ингибиторы комплементаб анти-ФНО ингибиторы) [39,40,41].
Клинические рекомендации при катастрофическом антифосфолипидном синдроме (КАФС).КАФС характеризуется вовлечением в патологический процесс многих органов за короткий период времени. Гистологическая картина проявляется наличием окклюзии мелких сосудов и лабораторными маркёрами в крови являются антифосфолипидные антитела (аФЛ) [42,43]. С точки зрения патофизиологии, КАФС – тромботическая микроангиопатия, характеризующаяся диффузной тромботической микроваскулопатией [44]. И хотя, частота КАФС составляет 1% из всех случаев АФС, они обычно представляют собой жизненно-угрожающие состояния в 30-50% случаев со смертельным исходом [44].
Предварительные классификационные диагностические критерии КАФС с диагностическим алгоритмом были разработаны в 2003г [43]. Для улучшения алгоритма и более точной диагностики КАФС был разработан пошаговый подход алгоритма КАФС [45]. В этот алгоритм был включен предшествующий анамнез наличия АФС или постоянная позитивность по аФЛ, число вовлечённых органов, время исхода, наличие микротромбозов по данным биопсии и другие данные, позволявшие объяснить причину множественных тромбозов.
Информация, основанная на доказательной базе, приводится в четырёх ретроспективных исследованиях, анализировавших КАФС регистр [46,47,48,49]. Наиболее важные заключения по терапии КАФС сводятся к следующим выводам:1. Высокий уровень выздоровления достигается при комбинации антикоагулянтов (АК) с ГК плюс плазмаобмен (плазмаферез (ПФ) (77,8% против 55,4% при отсутствии подобной комбинации р=0,083), следующей за антикоагулянтной терапией плюс ГК, плюс ПФ и/или в/в иммуноглобулин (69% против 54,4% при отсутствии подобной комбинации р=0,089).2. Изолированнное использование ГК было связано с низким уровнем выздоровления (18,2% против 58,1% эпизодов не леченных ГК).3. Использование циклофосфамида (ЦФ) улучшало выживаемость больных КАФС на фоне СКВ [47].4. Уровень смертности уменьшился с 53% у больных с КАФС до 2000 года до 33,3% у тех, кто перенёс КАФС с 2001 до февраля 2005г (р=0,005 , отношение шанса (ОШ) 2,25; 95% конфиденциальный интервал (КИ) 1,27-3,99) [46]. Главным объяснением подобного снижения уровня смертности было комбинированное применение АК+ГК+ПФ и/или в/в иммуноглобулин.
Исходя из вышеперечисленных выводов, в терапевтическую стратегию КАФС рекомендуется включение идентификации и лечения любых сопутствующих факторов риска тромбоза (в первую очередь инфекций) и в терапии КАФС рекомендована комбинация АК с ГК плюс ПФ и/или в/в человеческий иммуноглобулин. При развитии КАФС на фоне СКВ в/в введение ЦФ [47] может быть рекомендовано при отсутствии противопоказаний и, особенно, при наличии других клинических проявлений СКВ.
Данные Международного регистра КАФС не дал ответы на спорные и неизвестные стороны этого варианта АФС. Первый и возможно наиболее важным неизвестным моментом является почему незначительное число больных с аФЛ развивают полиорганную недостаточность, называемого КАФС. Кроме того, распределение по возрасту, полу, связи с СКВ, профилю аФЛ у больных классическим АФС и КАФС схож [42]. С патофизиологической точки зрения КАФС является тромботическим микроангиопатическим состоянием, характеризующийся диффузной тромботической микроваскулопатией. Подобные патологические находки могут быть представлены и в других состояниях таких как тромботическая тромбоцитопеническая пурпура (ТТП), гемолитико-уремический синдром (ГУС), злокачественной гипертензии, HELLP –синдроме, послеродовой почечной недостаточности и преэкласмпсии. Тромботическая микроангиопатия, сопровождающаяся наличием аФЛ в крови, описывается во всех выше перечисленных состояниях, приводя к концепции «микроангиопатического антифосфолипид-ассоциированного синдрома» [50] и приводя к диагностическим поискам. Однако источник и патогенетический потенциал аФЛ в этих состояниях остаётся неизвестным; предполагается, что аФЛ могут вызывать пертурбацию и повреждение эндотелиальных клеток, что прводит к катастрофически исходом [51]. Ещё одним важным моментом должно быть идентификация АФС пациентов с высоким риском развития КАФС. Выявление и лечение преципитирующих факторов для предотвращения развития катастрофических эпизодов у больных с аФЛ является существенным [52]. Прекращение приёма антикоагулянтов или низкое медународное нормализованное отношение (МНО) было одним из подобных факторов у 8% больных с катастрофическими эпизодами [53], тем не менее доктора лечащие пациентов с АФС должны быть особенно внимательны в клинических ситуациях, когда приём антикоагулянтов следует прекратить, например при хиру
diseases.medelement.com
Антифосфолипидный синдром - анализы, диагностика и клинические рекомендации
Аутоиммунные заболевания сложно поддаются успешному лечению, поскольку клетки иммунитета вступают в борьбу с отдельными жизненно важными структурами организма. Среди распространенных проблем со здоровьем - фосфолипидный синдром, когда иммунная система воспринимает структурную составляющую кости, как инородное тело, стараясь истребить.
Что такое антифосфолипидный синдром
Любое лечение должно начинаться с диагностики. Антифосфолипидный синдром – это аутоиммунная патология с устойчивым противостоянием иммунитета по отношению к фосфолипидам. Поскольку это незаменимые структуры для формирования и укрепления костной системы, неправильные действия иммунитета могут негативно сказаться на здоровье, жизнедеятельности всего организма. Если в крови наблюдаются антифосфолипидные антитела, болезнь не протекает в одиночку, ее сопровождают венозные тромбозы, инфаркт миокарда, инсульт, хроническое не вынашивание беременности.
Указанное заболевание может преобладать в первичной форме, т.е. развивается самостоятельно, как единичный недуг организма. Синдром антифосфолипидный имеет и вторичную форму (ВАФС), т.е. становится осложнением другого хронического заболевания организма. Как вариант, это могут быть синдром Бадда-Киари (тромбоз печеночных вен), синдром верхней полой вены и прочие патогенные факторы.
Антифосфолипидный синдром у мужчин
Обширная медицинская практика описывает случаи заболевания представителей сильного пола, хотя таковы встречаются гораздо реже. Антифосфолипидный синдром у мужчин представлен закупоркой просвета вен, в результате чего нарушается системный кровоток в отдельных внутренних органах, системах. Недостаточное кровоснабжение может привести к таким серьезным проблемам со здоровьем, как:
- тромбоэмболия легочной артерии;
- легочная гипертензия;
- эпизоды ТЭЛА;
- тромбоз центральной вены надпочечников;
- постепенное отмирание легочной, печеночной ткани, паренхимы печени;
- не исключены артериальные тромбозы, нарушения со стороны органов ЦНС.

Антифосфолипидный синдром у женщин
Заболевание влечет за собой катастрофические последствия, поэтому врачи настаивают на немедленной диагностике, эффективном лечении. В большинстве клинических картин пациентки – представительницы слабого пола, причем не всегда беременные. Антифосфолипидный синдром у женщин является причиной диагностированного бесплодия, а результаты обследования на АФС показывают, что в крови сосредоточено огромное количество тромбов. Международный код МКБ 10 включает указанный диагноз, который чаще прогрессирует при беременности.
Антифосфолипидный синдром у беременных
При беременности опасность заключается в том, что при формировании сосудов плаценты развивается и стремительно прогрессирует тромбоз, который нарушает кровоснабжение плода. Кровь не обогащается в достаточном объеме кислородом, а эмбрион страдает от кислородного голодания, не получает ценные для внутриутробного развития питательные вещества. Определить недуг можно на плановом скрининге.
Если развивается антифосфолипидный синдром у беременных, для будущих мамочек это чревато преждевременными и патологическими родами, выкидышем на раннем сроке, фето-плацентарной недостаточностью, поздними гестозами, отслойкой плаценты, врожденными заболеваниями новорожденных. АФС при беременности – это опасная патология на любом акушерском сроке, которая может закончиться диагностированным бесплодием.
Причины антифосфолипидного синдрома
Определить этиологию патологического процесса сложно, а современные ученые по сей день теряются в догадках. Установлено, что синдром Снеддона (его же называют антифосфолипидным) может иметь генетическую предрасположенность при наличии локусов DR7, DRw53, HLA DR4. К тому же, не исключено развитие заболевания на фоне инфекционных процессов организма. Другие причины антифосфолипидного синдрома подробно изложены ниже:
- аутоиммунные заболевания;
- длительный прием медицинских препаратов;
- онкологические заболевания;
- патологическая беременность;
- патологии сердечно-сосудистой системы.
Симптомы антифосфолипидного синдрома
Определить заболевание можно по анализу крови, однако дополнительно предстоит провести еще ряд лабораторных исследований на обнаружение антигена. В норме в биологической жидкости его быть не должно, а появление лишь свидетельствует, что в организме идет борьба с собственными фосфолипидами. Основные симптомы антифосфолипидного синдрома подробно изложены ниже:
- диагностика АФС по сосудистому рисунку на чувствительных кожных покровах;
- судорожный синдром;
- сильные приступы мигрени;
- тромбоз глубоких вен;
- психические нарушения;
- тромбоз нижних конечностей;
- снижение остроты зрения;
- тромбоз поверхностных вен;
- надпочечниковая недостаточность;
- тромбоз вен сетчатки глаза;
- ишемическая нейропатия зрительного нерва;
- тромбоз воротной вены печени;
- нейросенсорная тугоухость;
- острая коагулопатия;
- рецидивирующие гиперкинезы;
- синдром деменции;
- поперечный миелит;
- тромбозы церебральных артерий.
Диагностика антифосфолипидного синдрома
Чтобы определить патогенез заболевания, положено пройти обследование на АФС, при котором требуется сдавать анализ крови на серологические маркеры – волчаночный антикоагулянт и антитела Ат к кардиолипину. Диагностика антифосфолипидного синдрома помимо сдачи анализов предусматривает антикардиолипиновый тест, АФЛ, коагулограмму, допплерометрию, КТГ. В основе диагностики лежат показатели крови. Чтобы повысить достоверность результатов, по рекомендации лечащего врача показан комплексный подход к проблеме. Итак, обратить внимание на следующий симптомокомплекс:
- волчаночный антикоагулянт увеличивает численность тромбозов, при этом сам был впервые диагностирован при системной красной волчанке;
- антитела к кардиолипину противостоят натуральным фосфолипидам, способствуют их стремительному разрушению;
- антитела, контактирующие с кардиолипином, холестерином, фосфатидилхолином, определяются ложноположительной реакцией Вассермана;
- бета2-гликопротеин-1-кофакторзависимые антифосфолипидные антитела становятся главной причиной симптомов тромбоза;
- антитела к бета-2-гликопротеину, ограничивающие шансы пациентки благополучно забеременеть.
- АФЛ-негативный подтип без обнаружения антител к фосфолипидам.
Лечение антифосфолипидного синдрома
Если диагностирован АФЛС или ВАФС, при этом признаки недуга выражены отчетливо без дополнительных клинических обследований, это означает, что лечение требуется начать своевременно. Подход к проблеме комплексный, включает прием медикаментов нескольких фармакологических групп. Основная цель – нормализовать системное кровообращение, предотвратить формирование тромбов с последующими застойными явлениями организма. Итак, основное лечение антифосфолипидного синдрома представлено ниже:
- Глюкокортикоиды в малых дозах для предотвращения повышенной свертываемости крови. Желательно выбирать медицинские препараты Преднизолон, Дексаметазон, Метипред.
- Иммуноглобулин для коррекции иммунитета, ослабленного длительной медикаментозной терапией.
- Антиагреганты необходимы для предотвращения свертываемости крови. Особенно актуальны такие медикаменты, как Курантил, Трентал. Не лишним будет прием аспирина и Гепарина.
- Непрямые антикоагулянты для контроля вязкости крови. Врачи рекомендуют медицинский препарат Варфарин.
- Плазмаферез обеспечивает очищение крови в условиях стационара, однако дозы указанных медикаментов положено снизить.
При катастрофическом синдроме антифосфолипидном положено увеличить суточную дозу глюкокортикоидов и антиагрегантов, в обязательном порядке проводить чистку крови с повышенной концентрацией гликопротеина. Беременность должна протекать под строгим врачебным контролем, иначе клинический исход для беременной женщины и ее ребенка не самый благоприятный.
Видео: что такое АФС
Информация представленная в статье носит ознакомительный характер. Материалы статьи не призывают к самостоятельному лечению. Только квалифицированный врач может поставить диагноз и дать рекомендации по лечению исходя из индивидуальных особенностей конкретного пациента.
sovets.net