Причины и механизм развития сепсиса, методы диагностики и лечения. Сепсис стадии
12.3. СЕПСИС
12.3. СЕПСИС
В IV в. до н.э. Аристотелем был введен термин "сепсис". С тех пор прошло около 2,5 тыс. лет, но до настоящего времени нет цельного представления о механизмах его развития (Ю.Н. Белокуров, А. Б. Граменицкий, В. М. Молодкин, 1983). Несмотря на достижения современной медицины, сепсис остается одной из наиболее сложных и недостаточно изученных общеклинических проблем (М. И. Кузин, Б. М. Костюченок, 1982; В. И. Стручков, В. К. Гостищев, Ю. В Стручков, 1984; А.А. Тимофеев, 1989,1993,1995; В.В. Мулькевич, 1995; В.Г. Центило и др., 1995 и др.). Известно, что многие зарубежные авторы термином "хирургический сепсис" или "раневой сепсис" называют обычно нагноение послеоперационных ран, а не генерализацию инфекции (Jansson, 1971 ; Callone, 1974 ; Archie, 1977). Применяются также такие термины, как "септическое состояние", "гнойно- септические заболевания", "общая инфекция" и др. М. И. Кузин и Б. М. Костюченок (1982) указывают, что широко распространенный термин "септицемия" нередко объединяется с понятием "бактеремия", хотя это далеко не одно и то же. Ранее сказанное значительно затрудняет понимание сути изучаемого вопроса и создает известные трудности при установлении критериев сепсиса. Мы считаем, что целесообразно применять старые, устоявшиеся в отечественной литературе термины: "сепсис", "септицемия", "септикопиемия".
Существуют определенные различия в трактовке понятия "сепсис". С точки зрения диагностики и лечения сепсис следует рассматривать как патологическое состояние, обусловленное непрерывным или периодическим поступлением в кровь микроорганизмов из очага гнойного воспаления, характеризующееся несоответствием тяжелых общих расстройств местным изменениям и часто образованием очагов гнойного воспаления в различных органах и тканях.
Сепсис является полиэтиологическим заболеванием. Его возбудителем может быть любой микроорганизм, но наиболее часто - стафилококк, кишечная и синегнойная палочка, протей, анаэробы, реже - стрептококк, пневмококк и другие микробы.
По мнению В. И. Стручкова и соавторов (1984), патогенез сепсиса определяется тремя факторами: микробиологическим - видом, вирулентностью, состоянием кровообращения в очаге; количеством и длительностью воздействия попавших в организм бактерий; местом внедрения инфекции, характером и объемом разрушения тканей, состоянием иммунобиологических сил организма.
В зависимости от различных сочетаний перечисленных факторов сепсис может быть острейшим (молниеносным), обусловленным распространением высокопатогенных микроорганизмов и характеризующийся крайне тяжелым и быстрым течением; острым - с развитием выраженной клинической картины болезни в течение нескольких дней и отсутствием ремиссий, подострым - проявляющимся преимущественно возникновением метастатических абсцессов и менее выраженными общими нарушениями; хроническим - медленно текущим процессом с длительными, до нескольких месяцев и даже лет, периодами ремиссий между образованием очагов воспаления в различных органах и тканях.
Ранние формы сепсиса протекают по типу аллергической реакции и развиваются у больных, находящихся в состоянии сенсибилизации (Ю.Г Шапошников и соавт., 1974; С.М. Курбангалеев, Б. Б. Владимиров, 1975). В развитии позднего сепсиса при обширном и длительно текущем процессе играет роль постоянное поступление в организм больного токсинов и продуктов распада тканей, что приводит к изменению его реактивности, развитию состояния сенсибилизации (В.И. Стручков и соавт., 1984). Ограничение инфекции на ранних этапах заболевания осуществляется преимущественно за счет местного иммунитета.
Летальность при сепсисе колеблется от 35% до 69% случаев, в зависимости от его форм и вида возбудителя (М.И. Кузин и соавт., 1982; А.А. Тимофеев и соавт., 1987 и др.).
Септический процесс, развивающийся в челюстно- лицевой области, подразделяют на:
• одонтогенный - первичный очаг гнойного воспаления находится в периодонте;
• стоматогенный - очаг гнойного воспаления расположен в тканях слизистой, ок-ружающих ротовую полость;
• раневой - причиной развития являются инфицированные раны;
• тонзиллогенный - гнойник расположен в области миндалин или окологлоточном клетчаточном пространстве;
• риногенный - источник расположен в носовой полости;
• отогенный - очаг гнойного воспаления находится в среднем ухе.
В истории развития учения о "ротовом" сепсисе А.И. Рыбаков и соавт. (1983) выделяют три основных этапа.
До 50-х годов для профилактики сепсиса считали непременным условием удаление всех зубов с осложненным кариесом. В то же время при острых воспалительных процессах врачи боялись удалять причинные зубы, так как без применения при хирургическом вмешательстве активной антибактериальной терапии развивались опасные осложнения.
Период с 50-х до конца 60-х годов характеризуется успешным применением антибиотиков. В это время такое осложнение наблюдалось значительно реже.
С 70-80-х годов вновь наблюдался рост этой патологии. Основным первичным источником гнойно- некротических процессов челюстно- лицевой области у 99% больных являются очаги одонтогенной инфекции, возникшие как следствие кариеса зубов.
Частота одонтогенного сепсиса колеблется от 0,87 до 6,6% (С.Д. Сидоров, 1977) и составляет 2,2% от числа госпитализированных больных с острой одонтогенной инфекцией (В.А. Козлов, 1979).
В нашей клинике этот вид осложнения встречался у 0,3% больных, госпитализированных с воспалительными заболеваниями челюстно- лицевой области и шеи.
Для генерализации инфекции, по мнению М.И. Кузина и соавторов (1981), необходимо наличие в очаге воспаления определенного количества микробных тел, так называемого критического уровня бактериальной обсемененности (105 микробов на 1 г ткани).
Экспериментально доказано (Elek, 1956), что для распространения гнойной инфекции в нормальных тканях необходимо ввести в них от 2 000000 до 8 000000 стафилококков. Если через ткани в месте инъекции микробов провести обычную нитку, то "критическое" число микробов уменьшается до 10000, а при затягивании этой нити - до 100. "Критическое" число микробов значительно уменьшается при воздействии на ткани механических факторов, при шоке и ослаблении иммунологической реактивности организма (Д. Александер, Р. Гуд, 1974). Результаты клинико-бактериологических исследований, проведенных Krizek, Robson (1975), свидетельствуют о том, что в ранах, содержащих свыше 105 бактерий в 1 г ткани, возникает развитие гнойно-воспалительного процесса.
Многообразие форм и клинических проявлений сепсиса создают значительные трудности для его систематизации. Классифицируют сепсис по фазам: начальная фаза сепсиса (токсемия), септицемия (бактериемия без гнойных метастазов) и септикопиемия (постоянная бактериемия с гнойными метастазами). До настоящего времени одним из наиболее сложных вопросов в трактовке общих проявлений воспалительных процессов остается вопрос о правомочности термина "гнойно- резорбтивная лихорадка". По мнению М.И. Кузина и соавторов (1979), гнойно- резорбтивную лихорадку следует отнести к начальной форме проявления сепсиса. Они называют ее "предсепсисом". В.Г. Бочоришвили и соавторы (1981) выделяют несколько вариантов так называемого предсепсиса: затяжной субфебрилитет с постоянным или относительно быстрым переходом в высокую (нередко гектическую) лихорадку; "беспричинные" однодневные (чаще длящиеся 2-3 ч) подъемы температуры тела с ознобом и последующим проливным потом. Эти явления могут продолжаться 3-4 недели, а затем интервал между подъемами температуры уменьшается и лихорадка принимает гектический, ремиттирующий или постоянный характер. В течение довольно длительного времени (от 1 до 3 мес) подъем температуры чередуется с ее спадом.
Гнойно- резорбтивная лихорадка - это общий синдром, который тесно связан с местным нагноительным процессом и обусловлен всасыванием токсических продуктов из очага гнойного воспаления. Она характерна для всех гнойно- воспалительных заболеваний челюстно-лицевой области и может наблюдаться в течение 7 суток после вскрытия гнойного очага. Посевы крови у больных с гнойно- резорбтивной лихорадкой обычно стерильны. Первым предложил выделять данный синдром И. В. Давыдовский (1944). В развитии гнойно- резорбтивной лихорадки основную роль играет всасывание продуктов белкового распада и бактерий. Резорбция происходит лимфогенным и гематогенным путем. Длительное течение этой лихорадки может привести к ослаблению общей и специфической иммунологической реактивности организма. Одновременно с всасыванием токсических продуктов происходит большая потеря с гноем белков, ферментов и других веществ. При типичном удалении периодонтитного зуба, по данным Е. Сабо (1977), у 70% больных в циркулирующей крови можно обнаружить бактерии. Эта бактеремия через несколько часов прекращается. Однако в некоторых случаях бактеремия и токсемия может продлиться 3-4 дня.
Большие трудности при проведении дифференциальной диагностики между сепсисом и гнойно- резорбтивной лихорадкой в ранние сроки их развития отмечают многие авторы В случае, если после устранения гнойного очага и проведения адекватной противовоспалительной медикаментозной терапии общие проявления не устраняются и наблюдается кратковременная бактериемия, то следует думать, что у больного возникла начальная фаза сепсиса. Несмотря на активное воздействие на гнойный очаг, общее состояние больного ухудшается, температура тела повышается до 39-4СРС (с большими колебаниями в течение суток), появляется озноб, сильная головная боль, тахикардия, тахипноэ, бессонница. Если из крови высевается патогенная микрофлора, то это указывает на развитие септицемии. На этой стадии развития сепсиса не удается выявить гнойные метастатические очаги. Когда на фоне клинических проявлений септицемии появляются гнойные метастатические очаги в различных органах и тканях, то это указывает на развитие следующей стадии сепсиса - септикопиемии.
Клиническая картина при сепсисе резко ухудшается. У больного возникают возбуждение или подавленность, желтушность кожных покровов, покраснение щек, глаза становятся блестящими, губы - сухими и яркими, язык обложен, пульс учащается и постепенно уменьшается его наполнение. При крайне тяжелых формах наблюдается геморрагический синдром: кровоизлияние на местах инъекций и легчайших травм, геморрагии в зеве, носовые кровотечения, рвота с примесью алой крови или в виде кофейной гущи, кровавый понос, микро- и макрогематурия (Т.В. Жернакова, 1981). Характерны изменения как красных, так и белых форменных элементов крови. Сепсис сопровождается быстро нарастающей анемией, которая выявляется клинически (бледностью кожных покровов и мягкого нёба, иктеричность склер и др.), и в анализах крови (уменьшение числа эритроцитов и содержания гемоглобина). Анемия возникает в результате угнетения эритропоэза. Наиболее характерными изменениями белых форменных элементов крови при сепсисе является выраженный лейкоцитоз с нейтрофильным сдвигом влево (резкое "омоложение" лейкоцитов), появление токсической зернистости лейкоцитов. СОЭ увеличивается более 50 мм/ч. Изучение активности свертывающих фибринолитических свойств крови у больных сепсисом позволило Л.П. Мальчиковой и ГА. Красковской (1982) выявить глубокие изменения в системе гемокоагуляции. При этом патологическом состоянии авторами отмечено увеличение глобулиновых фракций крови. По их мнению, это может влиять на повышение протеолитической активности крови, ибо известно, что белок, защищающий протеолитические ферменты от действия ингибиторов, находится в основном в альфа -2- глобулиновой фракции.
Тяжелейшим осложнением сепсиса является септический шок. Он возникает вследствие воздействия на организм больного бактериальных токсинов и выражается в глубоких изменениях функций всех его систем, из которых на первый план выступает нарушение кровообращения, дыхания, недостаточное обеспечение тканей организма кислородом. За последнее десятилетие частота случаев септического шока увеличилась в 2-3 раза.
Пусковым механизмом развития септического шока является выраженная бактериемия с последующим выделением в кровь значительного количества бактериальных эндотоксинов. При этом состоянии отмечена фрагментация красных кровяных клеток, что рассматривается как следствие диссеминированного внутрисосудистого свертывания (М.И. Кузин и соавт., 1983). Авторами выявлено, что возникновение пойкилоцитоза при сепсисе обусловлено бактериальной интоксикацией. В результате непосредственного или опосредованного действия бактериальных токсинов на эритроцитарные мембраны изменяются физико-химические свойства липидного биослоя этих форменных элементов.
Синдром диссеминированного внутрисосудистого свертывания (ДВС) крови представляется, как динамический биологический процесс, в основе которого лежит рассеянное и часто повсеместное свертывание крови, ведущее к блокаде микроциркуляции, развитию тромботических процессов и геморрагии, гипоксии тканей, тканевому ацидозу и глубокому нарушению функций органов.
В.Н. Гирин и соавт. (1992) выделяют четыре стадии ДВС синдрома.
• 1-я стадия (тромбоцитопеническое состояние) характеризуется усиленным тромбообразованием и признаками возрастающей гиперкоагуляции. При острой и значительной активности свертывания крови (хирургическая патология) она кратковременна.
• 2-я стадия характеризуется диссоциацией коагулограммы: с одной стороны отмечается усиление тромбообразования, снижение числа тромбоцитов, уменьшение содержания фибриногена, протромбина и других факторов свертывания крови, с другой - усиление фибринолиза; развивается так называемая коагулопатия потребления. В основе клинической картины этой фазы лежит геморрагический синдром.
• 3-я стадия - фаза дефибринации. Она характеризуется активацией противосвертывающей системы, снижением всех факторов свертывания крови, повышением уровня плазмина. При этом геморрагические явления усиливаются; кроме экхимозов наблюдаются паренхиматозные кровотечения.
• 4-я стадия называется восстановительной или стадией остаточных явлений.
Как правило, в развитии ДВС крови стадийность сохраняется, но при правильной и своевременной терапии может остановиться на 1-й или 2-й стадии.
По мнению В.Н. Гирина и соавт. (1992) диагноз ДВС синдрома можно установить на основании клинических проявлений, патологоанатомического исследования и подтвердить лабораторными тестами.
При 1-й стадии ДВС синдрома отмечается укорочение времени свертывания крови, времени рекальцификации плазмы и укорочение времени генерации тромбопластина, увеличение адгезивной способности тромбоцитов и повышение потребления протромбина. Число тромбоцитов нормально. Активность протромбина, факторов V, VIII, IX, X может быть несколько повышенной, как и концентрация фибриногена.
2-я стадия характеризуется с одной стороны ускорением реакции тромбопластинообразования, с другой началом потребления факторов свертывания крови, тромбоцитов, а также активацией фибринолиза. Тяжесть тромбоцитопении и снижение фибриногена на фоне повышения антикоагулянтной и фибринолитической активности свидетельствует о глубине патологического процесса в этой фазе.
При 3-й стадии имеется выраженная тромбоцитопения со значительным снижением фибриногена, протромбина, факторов V, VIII, XIII. Высокая фибринолитическая активность, сопровождающаяся значительным количеством продуктов распада фибриногена.
Для 4-й стадии характерно восстановление активности всех факторов свертывания крови.
Разделение стадий ДВС синдрома можно провести дополнительно с помощью клинических симптомов. 1-я стадия синдрома характеризуется блокадой микроциркуляции и явлениями гиперкоагуляции. При этом кожа бледной окраски, отмечается "мраморный" рисунок, акроцианоз, цианоз носогубного треугольника, тахикардия, тахипноэ, олигурия, гемоколит, тромбирование игл во время инъекций. При 2-й стадии на фоне ухудшения микроциркуляторных расстройств присоединяются симптомы коагулопатии потребления и активации фибринолиза: гемоколит, гематурия, рвота "кофейной гущей", кровоточивость из мест инъекций, петехиальные кровоизлияния на коже. 3-я стадия ДВС синдрома характеризуется глубокими нарушениями функции жизненно важных органов и кровотечениями. У больных имеет место нарушения сознания, судороги, почечная, дыхательная и сердечно- сосудистая недостаточность, а также носовые, желудочно-кишечные, почечные, маточные и другие кровотечения.
Морфологические признаки позволили В.Н. Гирину и соавт. (1992) выделить следующие стадии ДВС синдрома;
• 1-я стадия - гиперкоагуляции, характеризуется наличием множественных микротромбов различного строения;
• 2-я стадия - коагулопатия потребления, характеризуется преобладанием процессов гипокоагуляции в виде кровотечения или геморрагического диатеза; наличие тяжей и нитей фибрина в синусах печени и селезенки;
• 3-я стадия - активация фибринолиза, морфологически диагностируется довольно трудно. Наиболее характерно для этой стадии преобладание "гиалиновых" микротромбов;
• 4-я стадия - восстановительная или остаточных явлений блокады сосудов, характеризуется выраженными дистрофическими и некротическими изменениями в тканях и органах
Согласно выделенным стадиям В.Н. Гирин и соавт. (1992) предлагают осуществлять следующую терапию:
В 1-й фазе ДВС синдрома (гиперкоагуляция). Лечение гепарином начинают с подбора индивидуальной дозы препарата. Первая доза является 100 ЕД/кг массы тела. Через 4 часа проводят определение свертывания крови. Если последняя увеличилась в 2 раза, то доза гепарина считается эффективной, а если не изменилась, то дозу увеличивают на 50 ЕД/кг массы тела. Если же время свертывания крови превышает 15 минут, то дозу препарата уменьшают на 25 ЕД/кг массы тела. После подбора индивидуальной дозы гепаринотерапию продолжают в этом же режиме до прекращения внутривенных инфузий.
Реополиглюкин (10 мл/кг массы) - кровозаменитель гемодинамического действия, способствует дезагрегации и потенцированию действия гепарина.
Глюкоза-никатиново-новокаиновая смесь (глюкозы 10% - 100,0, никотиновой кислоты 1% - 1,0, новокаина 0,25% - 100,0) из расчета 10 мл/кг массы. Эта смесь улучшает микроциркуляцию. Новокаин воздействует на интерорецепторы сосудов в очаге поражения, оказывает спазмолитическое действие и нормализует проницаемость сосудов. Никотиновая кислота повышает активность тканевого и плазменного активатора фибринолизина.
Гидрокортизон (салукортеф) в повышенных дозах. В этих дозах препарат восстанавливает микроциркуляцию и обладает мембраностабилизирующим действием (8-10 мг/кг массы).
Дроперидол, эуфиллин. Доза этих препаратов в 1-й фазе ДВС синдрома может быть повышенной.
Во 2-й фазе ДВС синдрома (гипокоагуляции) в комплекс терапии дополнительно вводят следующие препараты.
Свежезамороженная плазма в дозе 10-15 мл/кг массы тела.
Ингибиторы трипсина, плазмина, калликреина - контрикал, трасилол, ингидрил, ам-бен, гордокс, аминокапроновая кислота в терапевтических дозах. Они угнетают фибринолиз на короткий срок, выводятся через 4 часа, поэтому их введение необходимо повторять несколько раз.
Препараты кальция (глюконата) в максимальных возрастных дозировках (3-10 мл 10% раствора) дробно в период проведения инфузионной терапии с целью коррекции агрегации тромбоцитов.
Гормоны (гидрокортизон, преднизолон) в обычных дозах.
При гипокоагуляции с выраженным фибринолизом, что клинически сопровождается повышенной кровоточивостью, авторы рекомендуют дополнительно назначать: альбумин (5-10 мл/кг массы), который оказывает антифибринолитический эффект, поскольку ингибиторы факторов фибринолиза относятся к альбуминовой фракции белков плазмы, понижает проницаемость сосудов; ингибиторы протеаз путем непрерывной инфузий; на фоне максимальных доз ингибиторов протеаз показано назначение антигистаминных препаратов, учитывая, что ингибируется не только фибринолиз, но и калликреин-кининовая система и свертываемость крови, доза гепарина снижается вдвое.
При низких показателях фибриногена крови необходимо вводить фибриноген внутривенно капельно (0,25-0,5 г) через 15-30 минут после введения гепарина.
При анемии показано переливание свежей донорской одногруппной крови дробно (по 20 мл через 6-8 часов) или отмытые эритроциты (в альбумине или реополиглюкине).
В случае продолжающегося геморрагического синдрома применяются внутривенные капельные вливания криопреципитата плазмы. Применяют свежезамороженную викасольную плазму и другие гемостатики (андроксон, дицинон, витамин К).
В заключении мне хотелось бы остановиться на отличительных особенностях общехирургического и одонтогенного сепсиса.
При одонтогенном сепсисе, как правило, имеется первичный гнойный очаг. Криптогенный сепсис, то есть процесс, при котором первичный очаг гнойного воспаления оставался нераспознанным, в нашей практике не встречался. Клинические проявления одонтогенного воспалительного очага очень характерны и доступны для диагностики. Другими словами, распознавание первичного одонтогенного гнойного очага трудностей обычно не представляет, диагностические ошибки крайне редкие.
Возбудителем инфекции обычно является стафилококк и его разновидности, развивающиеся как в монокультуре, так и в ассоциациях с другой кокковой флорой. Синегнойная палочка, протей, кишечная палочка, энтерококк и другие условно- патогенные микроорганизмы, характерные для общехирургических стационаров, в нашей практике обычно не встречаются. Возбудителем гнойных одонтогенных воспалительных процессов чаще является аутоинфекция, которая длительное время (в течение многих лет) находится (персистирует) в хронических очагах челюстно- лицевой области, манифестируя только в период обострений. Кстати, это обстоятельство еще раз весьма убедительно подчеркивает необходимость санации полости рта и носа, особенно у лиц, которым предстоит оперативное вмешательство в любой области тела.
В последние годы в общемедицинской практике стафилококк несколько потеснен анаэробной инфекцией, в частности клостридиями, которые также относятся к условно- патогенной микрофлоре. Распознавание этих возбудителей затруднено. В клинике для определения анаэробной микрофлоры приходится пользоваться косвенными признаками. Прежде всего, это локализация патологического очага в местах естественного обитания этой микрофлоры (полость рта, носовая часть глотки), зловонный запах экссудата, нередко с пузырьками газа, темный или даже черный цвет отделяемого и пораженных тканей, что определяется во время вскрытия гнойного очага. На рентгенограммах можно обнаружить пузырьки газа в виде множественных мелких гомогенных очагов разрежения тканей округлой формы, с четкими границами, в частности при медиастинитах в надключичной и в надгрудинной областях (рис. 12.2.1). Для анаэробной микрофлоры характерно отсутствие какого-либо положительного эффекта от применения массивных доз антибиотиков широкого спектра действия. Более того, длительное назначение аминогликозидов (гентамицин, канамицин, мономицин и др.) является фоном для развития анаэробной инфекции (A.M. Солнцев, А.А. Тимофеев, 1989).
Таким образом, одна из существенных особенностей одонтогенного сепсиса - это аутоинфекция.
К следующей особенности одонтогенного сепсиса следует отнести специфические пути распространения инфекции, которые обусловливают весьма характерные патологические процессы, предшествующие ему. Инфекция распространяется по лимфатическим сосудам в регионарные лимфатические узлы, вызывая лимфаденит, периаденит и аденофлегмону. При этом поверхностных лимфангоитов не наблюдается. Иногда удается распознать глубокий лимфангоит по ходу лицевой вены. Второй путь распространения инфекции - флебит вен лица: лицевой, ангулярной, верхне- и нижнеглазничных вен.
Возникновению одонтогенного сепсиса обязательно предшествует (помимо наличия гнойного очага в челюсти) лимфаденит с его осложнениями, абсцессы и флегмоны, а также флебит вен лица.
При локализации гнойного очага в подвисочной ямке он может быть своевременно не распознан, так как анатомически подвисочная ямка ограничена с трех сторон костными стенками, а снаружи - мощными мышечно-фасциальными массивами жевательной мускулатуры. Поэтому кожные покровы остаются неизмененными, припухлость мягких тканей не выражена, флюктуация не определяется. Эти затруднения в диагностике возникают, как показал наш опыт, чаще у врачей, оказывающих амбулаторную помощь. В 1986 г. мы наблюдали сепсис у 9 больных, из которых 6 погибли. С 1987 по 1996 гг. мы устанавливали и подтверждали сепсис у 26 больных (погибло 8). В основном это были люди молодого возраста, только двум было более 70 лет. Все больные поступили в стационар в порядке неотложной помощи с острыми одонтогенными воспалительными заболеваниями. У семи больных сепсис был диагностирован при поступлении, у остальных - через несколько дней. У 70% больных сепсис сочетался с медиастинитом. Заслуживает внимания тот факт, что обычное лечение, которое применяется у больных с острыми одонтогенными воспалительными заболеваниями, у всех оказалось недостаточно эффективным. Удаление причинного зуба и вскрытие гнойного очага не улучшило общее состояние и не привело к нормализации температуры тела. Интенсивная антибактериальная, дезинтоксикационная терапия и проведение всего комплекса противовоспалительного лечения оказались успешными у 75% больных (у 15% выздоровление наступило только через 2-3 месяца).
Прогноз при одонтогенном сепсисе, как и при других его видах, до сих пор остается весьма неблагоприятным.
studfiles.net
причины, симптомы, диагностика и лечение
Сепсис (заражение крови) – вторичное инфекционное заболевание, вызванное попаданием патогенной флоры из первичного локального инфекционного очага в кровяное русло. Сегодня ежегодно в мире диагностируется от 750 до 1,5 млн. случаев сепсиса. По статистике, чаще всего сепсисом осложняются абдоминальные, легочные и урогенитальные инфекции, поэтому данная проблема наиболее актуальная для общей хирургии, пульмонологии, урологии, гинекологии. В рамках педиатрии изучаются проблемы, связанные с сепсисом новорожденных. Несмотря на использование современных антибактериальных и химиотерапевтических препаратов, летальность от сепсиса остается на стабильно высоком уровне – 30-50%.
Классификация сепсиса
Формы сепсиса классифицируются в зависимости от локализации первичного инфекционного очага. На основании этого признака различают первичный (криптогенный, эссенциальный, идиопатический) и вторичный сепсис. При первичном сепсисе входные ворота обнаружить не удается. Вторичный септический процесс подразделяется на:
- хирургический – развивается при заносе инфекции в кровь из послеоперационной раны
- акушерско-гинекологический – возникает после осложненных абортов и родов
- уросепсис – характеризуется наличием входных ворот в отделах мочеполового аппарата (пиелонефрит, цистит, простатит)
- кожный – источником инфекции служат гнойные заболевания кожи и поврежденные кожные покровы (фурункулы, абсцессы, ожоги, инфицированные раны и др.)
- перитонеальный (в т. ч. билиарный, кишечный) – с локализацией первичных очагов в брюшной полости
- плевро-легочный – развивается на фоне гнойных заболеваний легких (абсцедирующей пневмонии, эмпиемы плевры и др.)
- одонтогенный – обусловлен заболеваниями зубочелюстной системы (кариесом, корневыми гранулемами, апикальным периодонтитом, периоститом, околочелюстными флегмонами, остеомиелитом челюстей)
- тонзиллогенный – возникает на фоне тяжелых ангин, вызванных стрептококками или стафилококками
- риногенный – развивается вследствие распространения инфекции из полости носа и придаточных пазух, обычно при синуситах
- отогенный - связан с воспалительными заболеваниями уха, чаще гнойным средним отитом.
- пупочный – встречается при омфалите новорожденных
По времени возникновения сепсис подразделяется на ранний (возникает в течение 2-х недель с момента появления первичного септического очага) и поздний (возникает позднее двухнедельного срока). По темпам развития сепсис может быть молниеносным (с быстрым развитием септического шока и наступлением летального исхода в течение 1-2 суток), острым (длительностью 4 недели), подострым (3-4 месяца), рецидивирующим (продолжительностью до 6 месяцев с чередованием затуханий и обострений) и хроническим (продолжительностью более года).
Сепсис в своем развитии проходит три фазы: токсемии, септицемии и септикопиемии. Фаза токсемии характеризуется развитием системного воспалительного ответа вследствие начала распространения микробных экзотоксинов из первичного очага инфекции; в этой фазе бактериемия отсутствует. Септицемия знаменуется диссеминацией возбудителей, развитием множественных вторичных септических очагов в виде микротромбов в микроциркуляторном русле; наблюдается стойкая бактериемия. Для фазы септикопиемии характерно образование вторичных метастатических гнойных очагов в органах и костной системе.
Причины сепсиса
Важнейшими факторами, приводящими к срыву противоинфекционной резистентности и развитию сепсиса, выступают:
- со стороны макроорганизма - наличие септического очага, периодически или постоянно связанного с кровяным или лимфатическим руслом; нарушенная реактивность организма
- со стороны инфекционного возбудителя – качественные и количественные свойства (массивность, вирулентность, генерализация по крови или лимфе)
Ведущая этиологическая роль в развитии большинства случаев сепсиса принадлежит стафилококкам, стрептококкам, энтерококкам, менингококкам, грамотрицательной флоре (синегнойной палочке, кишечной палочке, протею, клебсиелле, энтеробактер), в меньшей степени - грибковым возбудителям (кандидам, аспергиллам, актиномицетам).
Выявление в крови полимикробных ассоциаций в 2,5 раза увеличивает уровень летальности больных сепсисом. Возбудители могут попадать в кровь из окружающей среды или заноситься из очагов первичной гнойной инфекции.
Велико значение внутрибольничной инфекции: ее росту способствует широкое применение инвазивных диагностических процедур, иммуносупрессивных лекарственных препаратов (глюкокортикоидов, цитостатиков). В условиях иммунодефицита, на фоне травмы, операционного стресса или острой кровопотери инфекция из хронических очагов беспрепятственно распространяется по организму, вызывая сепсис. Развитию сепсиса более подвержены недоношенные дети, больные, длительно находящиеся на ИВЛ, гемодиализе; онкологические, гематологические пациенты; больные сахарным диабетом, ВИЧ-инфекцией, первичными и вторичными иммунодефицитами.
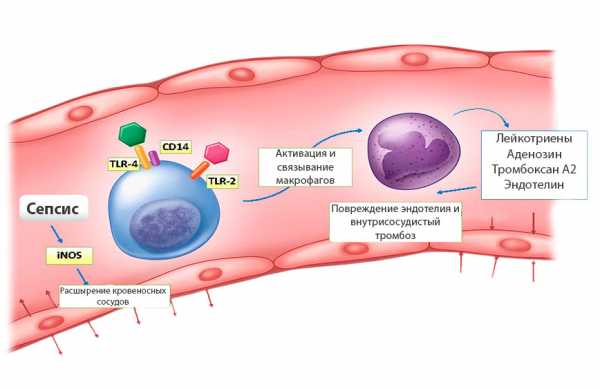
Механизм развития сепсиса многоступенчатый и очень сложный. Из первичного инфекционного очага патогены и их токсины проникают в кровь или лимфу, обуславливая развитие бактериемии. Это вызывает активацию иммунной системы, которая реагирует выбросом эндогенных веществ (интерлейкинов, фактора некроза опухолей, простагландинов, фактора активации тромбоцитов, эндотелинов и др.), вызывающих повреждение эндотелия сосудистой стенки. В свою очередь, под воздействием медиаторов воспаления активизируется каскад коагуляции, что в конечном итоге приводит к возникновению ДВС-синдрома. Кроме этого, под влиянием высвобождающихся токсических кислородсодержащих продуктов (оксида азота, перекиси водорода, супероксидов) снижается перфузия, а также утилизация кислорода органами. Закономерным итогом при сепсисе является тканевая гипоксия и органная недостаточность.
Симптомы сепсиса
Симптоматика сепсиса крайне полиморфна, зависит от этиологической формы и течения заболевания. Основные проявления обусловлены общей интоксикацией, полиорганными нарушениями и локализацией метастазов.
В большинстве случаев начало сепсиса острое, однако у четверти больных наблюдается так называемый предсепсис, характеризующийся лихорадочными волнами, чередующимися с периодами апирексии. Состояние предсепсиса может не перейти в развернутую картину заболевания в том случае, если организму удается справиться с инфекцией. В остальных случаях лихорадка принимает интермиттирующую форму с выраженными ознобами, сменяющимися жаром и потливостью. Иногда развивается гипертермия постоянного типа.
Состояние больного сепсисом быстро утяжеляется. Кожные покровы приобретают бледновато-серый (иногда желтушный) цвет, черты лица заостряются. Могут возникать герпетические высыпания на губах, гнойнички или геморрагические высыпания на коже, кровоизлияния в конъюнктиву и слизистые оболочки. При остром течении сепсиса у больных быстро возникают пролежни, нарастает обезвоживание и истощение.
В условиях интоксикации и тканевой гипоксии при сепсисе развиваются полиорганные изменения различной степени тяжести. На фоне лихорадки отчетливо выражены признаки нарушения функций ЦНС, характеризующиеся заторможенностью или возбуждением, сонливостью или бессонницей, головными болями, инфекционными психозами и комой. Сердечно-сосудистые нарушения представлены артериальной гипотонией, ослаблением пульса, тахикардией, глухостью сердечных тонов. На этом этапе сепсис может осложниться токсическим миокардитом, кардиомиопатией, острой сердечно-сосудистой недостаточностью.
На происходящие в организме патологические процессы дыхательная система реагирует развитием тахипноэ, инфаркта легкого, респираторного дистресс-синдрома, дыхательной недостаточности. Со стороны органов ЖКТ отмечается анорексия, возникновение «септических поносов», чередующихся с запорами, гепатомегалии, токсического гепатита. Нарушение функции мочевыделительной системы при сепсисе выражается в развитии олигурии, азотемии, токсического нефрита, ОПН.
В первичном очаге инфекции при сепсисе также происходят характерные изменения. Заживление ран замедляется; грануляции становятся вялыми, бледными, кровоточащими. Дно раны покрывается грязно-сероватым налетом и участками некрозов. Отделяемое приобретает мутный цвет и зловонный запах.
Метастатические очаги при сепсисе могут выявляться в различных органах и тканях, что обусловливает наслоение дополнительной симптоматики, свойственной гнойно-септическому процессу данной локализации. Следствием заноса инфекции в легкие служит развитие пневмонии, гнойного плеврита, абсцессов и гангрены легкого. При метастазах в почки возникают пиелиты, паранефриты. Появление вторичных гнойных очагов в опорно-двигательной системе сопровождается явлениями остеомиелита и артрита. При поражении головного мозга отмечается возникновение церебральных абсцессов и гнойного менингита. Возможно наличие метастазов гнойной инфекции в сердце (перикардит, эндокардит), мышцах или подкожной жировой клетчатке (абсцессы мягких тканей), органах брюшной полости (абсцессы печени и др.).
Осложнения сепсиса
Основные осложнения сепсиса связаны с полиорганной недостаточностью (почечной, надпочечниковой, дыхательной, сердечно-сосудистой) и ДВС-синдромом (кровотечения, тромбоэмболии).
Тяжелейшей специфической формой сепсиса является септический (инфекционно-токсический, эндотоксический) шок. Он чаще развивается при сепсисе, вызванном стафилококком и грамотрицательной флорой. Предвестниками септического шока служат дезориентация больного, видимая одышка и нарушение сознания. Быстро нарастают расстройства кровообращения и тканевого обмена. Характерны акроцианоз на фоне бледных кожных покровов, тахипноэ, гипертермия, критическое падение АД, олигурия, учащение пульса до 120-160 уд. в минуту, аритмия. Летальность при развитии септического шока достигает 90%.
Диагностика сепсиса
Распознавание сепсиса основывается на клинических критериях (инфекционно-токсической симптоматике, наличии известного первичного очага и вторичных гнойных метастазов), а также лабораторных показателях (посев крови на стерильность).
Вместе с тем, следует учитывать, что кратковременная бактериемия возможна и при других инфекционных заболеваниях, а посевы крови при сепсисе (особенно на фоне проводимой антибиотикотерапии) в 20-30% случаев бывают отрицательными. Поэтому посев крови на аэробные и анаэробные бактерии необходимо проводить минимум трехкратно и желательно на высоте лихорадочного приступа. Также производится бакпосев содержимого гнойного очага. В качестве экспресс-метода выделения ДНК возбудителя сепсиса используется ПЦР. В периферической крови отмечается нарастание гипохромной анемии, ускорение СОЭ, лейкоцитоз со сдвигом влево.
Дифференцировать сепсис необходимо от лимфогранулематоза, лейкемии, брюшного тифа, паратифов А и В, бруцеллеза, туберкулеза, малярии и других заболеваний, сопровождающихся длительной лихорадкой.
Лечение сепсиса
Пациенты с сепсисом госпитализируются в отделение интенсивной терапии. Комплекс лечебных мероприятий включает в себя антибактериальную, дезинтоксикационную, симптоматическую терапию, иммунотерапию, устранение белковых и водно-электролитных нарушений, восстановление функций органов.
С целью устранения источника инфекции, поддерживающего течение сепсиса, проводится хирургическое лечение. Оно может заключаться во вскрытии и дренировании гнойного очага, выполнении некрэктомии, вскрытии гнойных карманов и внутрикостных гнойников, санации полостей (при абсцессе мягких тканей, флегмоне, остеомиелите, перитоните и др.). В некоторых случаях может потребоваться резекция или удаление органа вместе с гнойником (например, при абсцессе легкого или селезенки, карбункуле почки, пиосальпинксе, гнойном эндометрите и др.).
Борьба с микробной флорой предполагает назначение интенсивного курса антибиотикотерапии, проточное промывание дренажей, местное введение антисептиков и антибиотиков. До получения посева с антибиотикочувствительностью терапию начинают эмпирически; после верификации возбудителя при необходимости производится смена противомикробного препарата. При сепсисе для проведения эмпирической терапии обычно используются цефалоспорины, фторхинолоны, карбапенемы, различные комбинации препаратов. При кандидосепсисе этиотропное лечение проводится амфотерицином В, флуконазолом, каспофунгином. Антибиотикотерапия продолжается в течение 1-2 недель после нормализации температуры и двух отрицательных бакпосевов крови.
Дезинтоксикационная терапия при сепсисе проводится по общим принципам с использованием солевых и полиионных растворов, форсированного диуреза. С целью коррекции КОС используются электролитные инфузионные растворы; для восстановления белкового баланса вводятся аминокислотные смеси, альбумин, донорская плазма. Для борьбы с бактериемией при сепсисе широко используются процедуры экстракорпоральной детоксикации: плазмаферез, гемосорбция, гемофильтрация. При развитии почечной недостаточности применяется гемодиализ.
Иммунотерапия предполагает использование антистафилококковой плазмы и гамма-глобулина, переливание лейкоцитарной массы, назначение иммуностимуляторов. В качестве симптоматических средств используются сердечно-сосудистые препараты, анальгетики, антикоагулянты и др. Интенсивная медикаментозная терапия при сепсисе проводится до стойкого улучшения состояния больного и нормализации показателей гомеостаза.
Прогноз и профилактика сепсиса
Исход сепсиса определяется вирулентностью микрофлоры, общим состоянием организма, своевременностью и адекватностью проводимой терапии. К развитию осложнений и неблагоприятному прогнозу предрасположены больные пожилого возраста, с сопутствующими общими заболеваниями, иммунодефицитами. При различных видах сепсиса летальность составляет 15-50%. При развитии септического шока вероятность летального исхода крайне высока.
Профилактические меры в отношении сепсиса состоят в устранении очагов гнойной инфекции; правильном ведении ожогов, ран, локальных инфекционно-воспалительных процессов; соблюдении асептики и антисептики при выполнении лечебно-диагностических манипуляций и операций; предупреждении госпитальной инфекции; проведении вакцинации (против пневмококковой, менингококковой инфекции и др.).
www.krasotaimedicina.ru
Сепсис
Сепсис – это общая гнойная инфекция, развивающаяся в результате попадания в организм патогенных микробов и продуктов их метаболизма.
Этиология и патогенез
Факторы развития сепсиса:
- Первичный очаг инфекции, расположенный близко к кровеносным сосудам
- Возбудитель, вирулентность, количество
- Реакция иммунитета (снижение, шок, возраст, большие кровопотери)
Классификация сепсиса
По возбудителю бывают сепсисы: стрептококковые, стафилококковые, менингококковые, смешанные и др.
По происхождению: сепсис из-за гнойной раны, послеоперационный в результате нарушения правил асептики, абдоминальный (воспалительные процессы в брюшной полости, абсцессы, перитонит), имплантационный, гинекологический, уросепсис.
По времени возникновения: Если сепсис развился в течение 14 дней с развития первичного очага инфекции – это ранний, если позже 14 дней – поздний.
По клиническому течению: молниеносный – симптомы развиваются очень быстро в течение первых суток, острый – развитие до нескольких суток, подострый – развивается в течение нескольких недель, хронический – годы ремиссий и обострений.
Стадии развития
- Токсико-резорбтивная лихорадка – синдром интоксикации, повышение температуры, в крови только токсины.
- Септицемия – появление и размножение в крови возбудителей
- Септикопиемия – заключительный этап. Образование во всем организме абсцессов.
Симптомы
- Высочайшая температура
- Профузный пот
- Потрясающий озноб
- Резкое снижение артериального давления
- Тахикардия
- Апатия или возбуждение
- Одышка
- Головная боль и бессонница
- Обезвоживание организма
- Развитие пролежней (при подостром и остром сепсисе), пневмонии.
Септический шок – острое расстройство кровообращения вследствие переполнения крови патогенной микрофлорой и выделение в нее свободных токсинов. Это неотложное состояние. Септический шок развивается внезапно: резко падает артериальное давление, нарастают тахикардия, одышка, нарушается функция почек – развивается олигурия, анурия, кожные покровы покрываются сыпью, петехиями, наблюдаются расстройства работы желудочно-кишечного тракта.
Тяжело протекает сепсис новорожденных. При этом виде сепсиса у малыша наблюдаются рвота, сильная диарея, отказ от бутылочки, груди мамы, ребенок худеет на глазах, очевидны симптомы обезвоживания: тургор кожи падает, она становится дряблой, морщинистой, цвет – землистый. В ряде случаев очаг первичной инфекции – нагноение пупочной ранки, вследствие неправильного ухода.
Лечение
Основные аспекты: подавить инфекцию и повысить сопротивляемость организма. При наличии ран – показано хирургическое иссечение пораженного, омертвевшего участка с последующей грамотной первичной хирургической обработкой, при абсцессах – вскрытие гнойников, карманов, дезинфекция полости, постановка дренажа с антисептическим раствором.
Всем больным сепсисом нужна интенсивная терапия: введение антибиотиков, в некоторых случаях достаточно больших доз, с четом предварительно выявленной чувствительности микроорганизмов, инфузионная терапия Гемодезом, Полидезом, Глюкозой.
Профилактика
Своевременное лечение первичных очагов инфекций, регулярная диспансеризация.
medihost.ru
Сепсис – что провоцирует опасное заболевание крови и эффективные методы лечения
Сепсисом называют тяжелейший воспалительный процесс, распространяемый полностью на весь организм, без ограничений, в основе которого всегда лежит гнойная микрофлора как возбудитель инфекции. Для заболевания характерен ряд специфических клинических признаков, таких как повышение общей температуры тела, учащение сердечного ритма, частоты дыхания и помраченного сознания. Кроме того, может преобладать симптоматика, связанная с конкретным видом микроорганизмов, явившихся возбудителем патологического состояния — тяжелый кашель на фоне пневмонии или дисфункции мочеобразования при тяжелой почечной недостаточности.
Характерной особенностью сепсиса любой этиологии является первичное развитие и размножение инфекции в какой-либо системе или органе, после чего возбудители которой проникают в общее кровяное русло и распространяются по всему организму на фоне общего снижения качества иммунитета, что и обуславливает непосредственно сепсис.
Механизм развития и наиболее вероятные источники распространения возбудителя
Наиболее распространенными первичными источниками развития сепсиса, в качестве ворот инфекции, служат легкие, органы брюшной полости и мочевыводящих путей, причем первое место занимает дыхательная система.
Кроме того, источником распространения общей инфекции могут стать:
- Очаги гнойных образований — хирургический сепсис.
- Акушерско-гинекологический, когда вратами инфекции становится слизистая оболочка матки.
- Ротовой сепсис, вызванный патологиями ротовой полости.
- Болезнь, взявшая начало из мочеполовой системы, носит название — уросепсис.
Возбудители, провоцирующие развитие сепсиса, чаще всего имеют бактериальное начало, однако встречается вирусный, грибковый и паразитарный сепсис. Ранее основными причинами развития патологии являлись грамотрицательные бактерии, однако современная хирургическая статистика за последнее десятилетие все чаще сталкивается с грамположительными микробами, вызывающими сепсис, самими яркими представителями которой являются стафилококки. На втором месте, по частоте встречаемости, находятся кишечная и синегнойная палочки, некоторые виды клебсиелл. Грибковый сепсис составляет примерно 5% от общей заболеваемости и вызывает чаще тяжелые формы болезни. Самым распространенным видом здесь являются виды кандид.
Распространение патогенной микрофлоры через центральную систему кровотока обеспечивает ее осаждение во всех органах и тканях, где возбудители продолжают свое патологическое воздействие. Развитие сепсиса возможно лишь при условии сниженного иммунитета, иначе защитно-барьерные системы организма подавляют патогенное воздействие возбудителей.
К группе особого риска относятся дети ранней возрастной группы и лица пожилого возраста. У первых иммунитет еще недостаточно развит, у вторых — наблюдается его снижение в силу возрастного старения кроветворной системы. Кроме того, иммунный ответ организма всегда ограничен при онкологических патологиях на фоне специфической терапии, сахарного диабета, крупного травматизма и ожогах, характеризующихся значительной площадью поражения.
Симптомы сепсиса и его разновидности
Наиболее часто встречающейся симптоматикой сепсиса, которая проявляется в большинстве клинических случаев, является повышенная, реже — пониженная у лиц старшей возрастной группы, температура тела, учащенное дыхание и сердечный ритм, помрачение рассудка и генерализованные отеки подкожной клетчатки. Кроме того, на ранних стадиях болезни, как правило, в первые часы после проникновения микроорганизмов в кровь пациента, отмечают тахикардию, пониженный уровень мочеиспускания и высокий уровень сахара в крови.
Признаками развитого сепсиса станут умопомрачение, метаболический ацидоз, приводящий, зачастую, к респираторному алкалозу, низкое кровяное давление, вследствие снижения системного сосудистого сопротивления, высокий сердечный выброс и недостаточность свертывания крови. Прогрессирующая гипотония, наблюдаемая при сепсисе, может привести к шоковому состоянию и галлюцинаторно-бредовому синдрому.
На общем фоне указанной симптоматики, отмечаются дополнительные клинические признаки, свойственные развитию бактериального генерализованного инфицирования:
- Крайне тяжелый внешний вид пациента, практически полная обездвиженность, особенно при острой и молниеносной формах болезни.
- Синюшность кожных покровов и наружных слизистых оболочек.
- Недостаточное капиллярное наполнение и холодность конечностей.
- Повышенная потливость.
- Увеличение лимфатических узлов по всему телу.
- Повышенная сонливость, особенно у детей и пожилых людей.
- Увеличение до гигантских размеров печени и селезенки.
- Локальные клинические признаки, характерные для определенного вида возбудителя, например сыпь при менингококковом сепсисе, перкуссионная тупость в области легких при пневмонии и так далее.
В зависимости от тяжести проявления клинических признаков и времени проявления дебюта болезни различают:
- Молниеносное течение сепсиса — специфическая симптомтика заболевания проявляется в течение до двух суток.
- Острое — до недели.
- Подострое — до двух недель.
- Хроническое — более месяца.
Стоит отметить, что для болезни, порой, характерно атипичное течение клинических признаков в виде некоторого сглаживания симптомов, что чаще проявляется на пике заболевания по причине угнетающего действия применяемых антибиотиков по схеме лечения.
Сепсис может протекать в различных формах:
- Септикопиемия
Образование множественных гнойниковых очагов на поверхности кожного покрова, либо во внутренних органах, в зависимости от степени обсеменения микробами мест локализации. Причем область гнойничкового распространения оказывает прямое влияние на клиническую картину — образование абсцессов в церебральных областях приводит к яркой симптоматике нарушений нервной деятельности, в области кишечника — сильным болям в брюшной полости и прогрессирующим нарушениям пищеварения.
Характеризующаяся особо агрессивным течением и спонтанностью проявления клинической картины, проявляется без наличия метастатических гнойных образований.
- Сепсис новорожденных, или пупочный сепсис
Отдельная форма болезни, выделенная по причине типичности и остроты симптоматики, развивающейся у новорожденных в первые дни жизни. Пупочный сепсис — особо тяжелая форма болезни младенцев, развивающаяся по причине генерализации воспалительных процессов из пупочного сечения. Для данной разновидности патологии характерны неудержимая рвота, понос, отказ от питания, молниеносное исхудание и обезвоживание. Наружные кожные покровы приобретают оттенок от темно-красного до черного, практически по всей площади тела ребенка. В области пупка наблюдают отдельные нагноения и абсцедирующие образования.
Независимо от формы, сепсис характеризуется сменой чередующихся состояний, которые имеют различный временной период в зависимости от остроты симптоматики и скорости распространения возбудителей по организму
- Синдром системной воспалительной реакции
Ранняя стадия болезни, для которой свойственно изменение температуры тела в обеих направлениях, пульсом выше 90 ударов в минуту, частотой дыхания выше 20 вдохов в минуту и изменениями лейкоцитарной формулы, также в обе стороны.
- Средняя степень
Сепсис характеризуется теми же клиническими проявлениями, что и предыдущая фаза, но с наличием в стерильных жидкостях организма возбудителей, вызвавших течение болезни. Так микроорганизмы обнаруживают в плазме крови, спинномозговой жидкости, моче и других. Симптоматика болезни начинает дополнятся признаками развивающихся пневмонии, воспаления брюшной полости, пурпуры и других локализованных процессов, места локализации которых возрастают в геометрической прогрессии.
- Тяжелая форма сепсиса
К предыдущему генезу добавляются признаки спонтанного снижения артериального давления, генерализованной отечности и наступающей дисфункции некоторых органов — в первую очередь страдает печень, почки и легкие, затем наступает очередь центральной нервной системы и пищеварительных механизмов желудка и кишечника.
- Септический шок
Характеризуется летальным исходом в каждом втором случае наступления данной фазы болезни. Смерть, как правило, наступает по причине острого нарушения кровообращения вследствие нарушения сердечного ритма и резкого падения артериального давления.
Методы диагностики и лечения сепсиса
Сепсис — клинический диагноз, для уточнения которого не требуется особых усилий или сложных лабораторных исследований. Существует определенный алгоритм действия, который проводят в условиях реанимации с целью уточнения механизмов, области распространения инфекции и вида возбудителя:
- Определение общей симптоматики болезни, основанной на анамнезе и первичном клиническом обследовании.
- Наличие, зачастую, повышенной температуры тела, определенной показателем выше 38,3 градусов.
- Пониженная температура тела, характерна, чаще, для молниеносной и острой формы болезни на ранних стадиях, либо вследствие терапевтического использования антибиотиков. Кроме того, такой феномен наблюдают у детей раннего возраста и лиц, старше 60-летнего возраста.
- Усиленная частота дыхательного процесса.
- Изменения, порой — весьма глубокие, психического состояния пациента.
- Значительные отеки иди положительный баланс жидкости с превышением на 20 мл в течение 24 часов.
- Повышенное количество глюкозы в плазме крови — выше 7,7 ммоль/л при условии отсутствия патологий диабетического ряда.
- Повышенное количество лейкоцитов — более 12 000 мкл −1.
- Наличие признаков генерализованного воспаления с более яркой симптоматикой в определенных областях.
- Нормологический лейкоцитоз, но с наличием преобладающего большинства — более 10% незрелых форм клеток.
- Повышенное содержание реактивного белка в плазме крови более, чем в два раза.
- Повышенное содержание в плазме про-кальцитонина более, чем в два раза.
- Снижение артериального давления. Систолический показатель менее 90 мм ртутного столба, диастолический — менее 40 мм. Либо давление снижено ровно в два раза относительно возрастной и половой нормы пациента.
- Прогрессирующие дисфункции жизненно важных систем и органов.
- Сниженное кислородное наполнение артериальной крови — PaO2 / FiO2 менее 300 мм ртутного столба.
- Острое снижение выделяемой мочи — часовой диурез менее 0,5 мл/кг даже при условии адекватной инфузионной терапии.
- Увеличение креатинина в сыворотке крови — более 44,2 мкмоль/л.
- Повышение тромбопластинового времени — более 60 секунд.
- Абсолютная кишечная непроходимость по причине отсутствия перистальтики.
- Снижение количества тромбоцитов — менее 100 000 мкл-1.
- Повышенная концентрация общего билирубина в крови — более 70 мкмоль/л.
- Высокое содержание лактатов в плазме крови, как показатель начавшихся процессов аутотоксикоза по причине накопления продуктов жизнедеятельности клеток — более 1 ммоль/л.
- Пониженной капиллярное наполнение и очаговое усиление цианоза, вплоть до почернения.
Все вышеуказанные симптомы и признаки являются типичными для проявления первых двух стадий развития сепсиса. Кроме того, различают дополнительные характеристики, свойственные для тяжелой формы болезни и шокового состояния:
- Сепсис-индуцированная гипотония в тех же рамках, что и по предыдущей симптоматике, но с тенденцией на спонтанное снижение, что и обусловлено наличием эпизодов;
- Нарушение деятельности легких. Кислородное наполнение артериальной крови менее 250 мм ртутного столба при отсутствии пневмонии и менее 200 мм — при ее наличии;
- Концентрация креатинина выше 176 мкмоль/л;
- Билирубина — более 34,2 мкмоль/л;
- Пониженная свертываемость крови в несколько раз.
С целью определения данных диагностических критериев, обязательно проводят следующие исследования:
- Расширенное определение лейкоцитарной формулы. Кроме анемических проявления и сдвигов лейкоцитарной формулы в обе стороны, могут наблюдаться панцитопения — при вовлечении в патологический процесс костного мозга и лимфоцитоз — в случае преобладания возбудителей вирусного ряда.
- Анализ мочи с обязательным забором образца для бактериологического исследования.
- Исследование почечной функции.
- Исследование сыворотки крови на определение концентрации альбуминов и других протеиновых образований.
- Исследование количества глюкозы в плазме крови.
- Тестирование на свертываемость крови — используются методы по определению качества D-димера и фибриногена.
- Бактериологические посевы крови пациента. Желательно проводить как можно скорее с целью скорейшего определения вида возбудителя и назначения корректной антибиотикотерапии.
- УЗИ и R-исследование органов брюшной полости с целью определения внутренних очагов инфекции и развивающейся дисфункции органов.
- Определение титра лактатов в сыворотке крови, а также — кислородного насыщения артериальной и венозной крови.
- Применение инвазивных методов — люмбальная пункция, бронхоскопия, лапароскопия, биопсия лимфатических узлов с целью основной локализации возбудителей.
Лечебные мероприятия при сепсисе требуют максимальной точности и скорости терапевтических действия в связи с быстрым распространением возбудителя по организму и особо тяжелым состоянием пациентов. Все лечебные процедуры проводятся строго в условиях реанимации — необходимо помнить, что у пациента равнозначная вероятность летального исхода и выживания.
Одно из ведущих мест в терапии сепсиса занимает поддерживающий уход. Пациентам, как правило, требуется:
- Искусственная вентиляция легких в сочетании с интубацией трахеи.
- Ударные дозировки внутривенной регидратации.
- Постоянный мониторинг артериального давления, частоты пульса и дыхательных движений;
- Мочевыводящая катетеризация.
- Возможное введение инсулина при условии слишком высокой концентрации глюкозы в плазме крови.
- В настоящее время, в отличие от терапии прошлых лет, не используется постоянное введение гидрокортизона с целью предотвращения инсулинового шока, если инфузионная и вазопрессорная терапия способны поддерживать стабильность гемодинамики. Гормональная терапия может быть применена у детей при абсолютной надпочечниковой недостаточности.
В качестве специфической терапии применяются следующие лечебные манипуляции:
- Внутривенное введение противомикробных средств, направленных на конкретные виды микроорганизмов, что определяется предварительными бактериологическими исследованиями видового состава микрофлоры. Если возможности своевременной видовой диагностики не случилось — возможно использование эмпирической комбинированной антимикробной терапии, но не более 3-5 дней. Кроме того, для пациентов с острым иммунным дефицитом, может потребоваться вменение противовирусных и противогрибковых препаратов;
- С целью борьбы против гипотонии применяют вазопрессин в ударных дозах, а также — добутамины, если отмечается сильная дисфункция сердечной деятельности.
- Группа сатинов, широко используемая при сепсисе любой формы, оказывает антиоксидантное, иммуномодулирующее и противовоспалительное действие, предотвращающее плейотропный апоптоз.
- Хирургическое лечение назначается в случае необходимости дренажа крупных очаговых абсцессов.
С целью предотвращения осложнений и скорейшего выхода пациента из тяжелого состояния, разработаны специальные меры в виде конкретной инструкции для врачей, которую необходимо соблюдать при поступлении пациента в отделение реанимации
- В течение первых трех часов:
- Измерение уровня лактатов в сыворотке крови.
- Взятие анализа крови на бактериальный посев.
- Внутривенное введение антибиотиков широкого спектра действия.
- Контроль за артериальнымдавлением.
- В течение шести часов должны быть завершены следующие мероприятия:
- Применение вазопрессоров в случае устойчивой гипотонии, если диастолические показатели ниже 65 мм ртутного столба;
- При отсутствии повышения артериального давления, дополнительно проводятся исследования на показатели центрального венозного давления и центрального венозного насыщения кислородом.
Возможные осложнения заболевания и прогноз
При поступлении в реанимационное отделение, пациенту отводят всего лишь 40% возможности к выживанию. Если первичные реанимационные мероприятия не были проведены должным образом — данный показатель увеличивается до 60% в связи с высоким риском появления септического шока. Ситуацию значительно отягощают попутные хронические болезни из анамнеза пациента. Правильный терапевтический подход, особенно на ранних стадиях сепсиса, обеспечивает выживаемость одного из шести пациентов с тяжелой формой болезни, в том числе — септическим шоком.
Риск летального исхода всегда выше у пожилых детей и лиц пожилого возраста, причем для этих категорий пациентов весьма высокое значение имеет, так называемая — долгосрочная смертность, которая наступает по истечении 90 дней после приема в условия реанимации. Таким образом, процент смертности у пожилых людей составляет 55% и у детей, в возрасте одного года и двух лет — 31% и 43% соответственно.
Факторами, являющимися причиной долгосрочной смертности, как правило, становятся — застойная сердечная недостаточность, заболевания периферических сосудов, осложненный диабет, деменция, чаще — сосудистого типа, а также — результат регулярное искусственной вентиляции легких. Стоит отметить, что отказ от курения и применение сердечных гликозидов значительно снижают уровень долгосрочной смертности.
После перенесенного сепсиса пациентов, как правило, очень длительное время — на протяжении нескольких лет, а то и пожизненно сопровождают рассеянное внутрисосудистое свертывание, хроническая надпочечниковая недостаточность, а также — полиорганная недостаточность, например хроническая недостаточность почек, сопряженная с кардиореспираторной дисфункцией.
www.operabelno.ru
Сепсис. Лечение, симптомы,признаки сепсиса и сепсис классификация
Сепсис — неспецифический инфекционный процесс, вызываемый чаще всего гноеродными возбудителями, характеризующийся изменением реактивности организма больного и протекающий обычно при особых иммунно-биологических условиях, неблагоприятных для больного. Заболевание может возникнуть первично или присоединиться к другому заболеванию. Самый опасный сепсис новорожденных и сепсис крови.
Сепсис симптомы, признаки сепсиса
Чаще всего заболевание вызывается стрептококками и стафилококками, реже пневмококками, кишечной палочкой и др. При Сепсисе нередко удается обнаружить бактерии в крови (бактериемия). Более постоянным признаком заболевания является общая интоксикация (токсинемия).
Сепсис патогенез. Источником сепсиса служит инфекционно-воспалительный очаг -септический очаг (инфицированная рана, остеомиелит, отит, ангина и т. д.), из которого микроорганизмы, токсические продукты их жизнедеятельности и основные продукты тканевого распада постоянно или периодически поступают в организм человека, обусловливая интоксикацию его, нарушение регулирующей функции центральной нервной системы, с последующим расстройством обмена и изменением реактивности организма.
История сепсиса. Нашими отечественными учеными доказано влияние центральной нервной системы на развитие и ход септических процессов (А. И. Абрикосов, А. В. Вишневский и др.). Распространение инфекции из очага идет по лимфатическим или кровеносным путям. В развитии сепсиса большую роль играет ряд факторов, неблагоприятно влияющих на реактивность организма: шок, значительная потеря крови, различные предшествующие инфекционные заболевания (пневмония, тифы, скарлатина и т. д.), недостаточное питание, авитаминоз, повторность травмы (ранения) и т. д. В развитии раневого сепсиса могут сыграть неблагоприятную роль несвоевременная и неполноценная обработка и возникает хирургический сепсис, обработка ран с оставлением в ране инородных тел (остатки одежды, земли, осколки снаряда и т. д.), запоздалое хирургического вмешательство (при гнойных осложнениях в ране), многократные ревизии раневого очага и частые перевязки, неудовлетворительная транспортировка больных, плохая иммобилизация конечности. В происхождении раневого сепсиса видную роль играет перенесенная после ранения анаэробная инфекция.
Сепсис классификация
В зависимости от локализации первичного очага инфекции заболевание различают:
1. Хирургический сепсис, имеющий своим источником хирургические заболевания (остеомиелит, карбункулы, флегмоны и др.). Выделяется особая форма хирургического сепсиса, возникающего после боевых ранений (раневой). К хирургической группе также должен быть отнесены сепсисы при послеродовой инфекции (пуерперальный), при абортах и воспалительных процессах в женских половых органах, сепсис матки (гинекологический сепсис), при урологических заболеваниях (уросепспс), при гнойном отите (отогенный).
2. Сепсис при внутренних болезнях (терапевтический),возникающий как осложнение инфекционных болезней или различных воспалительных процессов внутренних органов (пневмонии, ангины, холециститы и т. д.). Заболевание нередко сопровождается появлением гнойных метастазов в различных областях тела. Заболевание, протекающие без метастатических гнойных очагов, носит название септицемии, с метастатическими очагами — септикопиемии. При сепсисе наблюдается ряд глубоких изменений в различных органах: перерождение, тромбофлебиты, кровоизлияния и т. д.
Виды сепсиса, стадии сепсиса
Различают острую, подострую и хроническую форму сепсиса. Общее состояние больных при сепсисе чаще всего тяжелое. Температура при сепсисе обычно повышается, причем нередко имеются большие колебания ее в виде подъемов до 39-41° по вечерам и падение до 35-36° по утрам. При значительной слабости и общем истощении температура может быть незначительно повышенной или даже ниже нормы. Нередки ознобы (иногда потрясающие), а также обильные (проливные) поты, отмечается потеря аппетита, тошнота, иногда рвоты, довольно часто — поносы, трудно поддающиеся лечению. Больные с сепсисом находятся чаще всего в состоянии угнетения и общей подавленности, причем это состояние нередко прерывается периодами возбуждения и бреда. Иногда у больных сепсисом появляются головные боли и ригидность затылка, служащие проявлениями раздражения или воспаления мозговых оболочек (сепсис мозга). Нередки боли в суставах, иногда с выпотами. Отмечается ряд изменений со стороны сердечно-сосудистой системы: тоны сердца становятся глухими, иногда появляется систолический шум, пульс учащается до 120-140 ударов в минуту, артериальное давление падает. При сепсисе могут наблюдаться разлитые бронхиты и очаговые пневмонии, туберкулезный сепсис,
протекающие с невыраженной клинической картиной. Печень увеличивается, нередко наблюдается желтуха. Селезенка увеличена и болезненна. Отмечаются изменения со стороны мочи в виде падения, наличия в моче белка и цилиндров, что служит проявлением инфекционного нефроза. В ряде случаев в моче обнаруживаются эритроциты, что свидетельствует о развитии при сепсиса очаговых или диффузных нефритов. Последние чаще наблюдаются при подостром септическом эндокардите. Имеются изменения со стороны крови — уменьшение числа эритроцитов и падение гемоглобина (иногда до 20-30%), увеличение числа лейкоцитов (до 20000-25000), при некоторых формах сепсиса количество лейкоцитов нормально или даже уменьшено, отмечается ускоренная РОЭ до 30-50 мм и больше в час. Рана становится сухой, выделение гноя и рост грануляций прекращается, дно покрывается фибринозным налетом, появляются участки некроза грануляций. У септических больных нередки пролежни.При пиемии гнойные метастазы появляются иногда в большом количестве, обычно во внутренних органах или в подкожной и межмышечной клетчатке, в суставах, костях.
Диагноз сепсис
Диагноз сепсиса ставится по клинической картине и данным бактериологической исследованиях крови, для посевов крови на питательную среду ее берут в количестве 5-10 мл из подкожных вен руки или ноги. Сепсис прогноз всегда серьезен, в настоящее время благодаря применению пенициллина смертность от сепсиса значительно снизилась.
Сепсис лечение
Лечение сепсиса. Антибиотики при сепсисе белый стрептоцид, норсульфазол (1,0 7 раз в сутки). Применяется пенициллин внутримышечно от 200000 до 500000 ЕД в сутки или внутривенно в виде капельного вливания в физиол. растворе, переливание крови систематически небольшими дозами, особенно в стадии выздоровления. Рекомендуется также фаготерапия. Интравенозное вливание 40% раствора уротропина по 10 мл ежедневно 1—2 раза. При бессоннице показаны веронал, люминал, бромурал, по показаниям — сердечные средства. При наличии гнойных очагов (сепсис гнойный) рекомендуется возможно раннее оперативное вмешательство (вскрытие гнойных очагов, иногда ампутация). Необходима тщательная иммобилизация конечностей при наличии очагов поражения на них.
Уход за больным при сепсисе
За септическими больными должен быть организован тщательный уход, они должны находиться в светлых, просторных палатах. Необходимо наблюдение за кожей (профилактика пролежней) и полостью рта (протирание и полоскание рта после каждого приема пищи).Питание при сепсисе. Большое значение имеет организация питания в сутки больные должны получать не менее 2500 калорий в пище должны быть полноценные белки, углеводы, сахар, витамины С и В2. Рекомендуется применение алкоголя (водка, вино). Больные должны получать достаточное количество жидкости (2-3 л в сутки).
Уросепсис
Уросепсис — разновидность общего сепсиса. Уросепспс возникает вследствие гнойно-воспалительных заболеваний мочевых, внутренних половых органов, флегмоны тазовой клетчатки, остеомиелита костей таза после огнестрельных ранений или закрытых переломов (гинекологический сепсис). В крови и гное при уросепсисе обнаруживаются чаще всего кишечная палочка и стрептококк, реже – стафилококк (гонококковый сепсис). В клинической картине уросепсиса на первый план выступают симптомы сепсиса с наслоением того урологического заболевания, которое привело к общему заражению организма. Септические проявления появляются на фоне первичного заболевания и выражаются в ознобе, высокой температурой при сепсисе, бреде, появляется желтушность склер, кожи, депрессия, истощение, высокий лейкоцитоз вначале быстро сменяется лейкопенией, являющейся признаком крайне тяжелого течения болезни (тяжелый сепсис).
Лечение сепсиса: вскрытие и дренирование мочевых затеков, резекция костей таза, при гнойничковом поражении почки декапсуляция и дренирование лоханки. Общее лечение, как при сепсисе.
travmedicina.ru
что это такое, симптомы, лечение, последствия сепсиса
Сепсис – это своеобразная системная патогенетическая реакция организма человека на внедрение инфекционного агента, развивающаяся как результат генерализации инфекционного воспалительного процесса на фоне выраженного снижения функции иммунного аппарата.
Острый сепсис у человека дебютирует при распространении инфекционного процесса из первичного очага, в качестве которого может выступать ограниченный нагноительный очаг, локализующийся в мягких тканях, внутренних органах, суставах и даже костной ткани. Сепсис у взрослого человека развивается, как правило, при выраженном снижении иммунитета, а также при несвоевременном распознании первичной локализации и этиологии воспалительного процесса, в результате чего наблюдается рассеивание токсических веществ по всему организму с током крови.
Инфекционный сепсис не следует рассматривать как контагиозную инфекцию, то есть данная патология не склонна передаваться каким-либо из известных способов передачи инфекционных агентов. Гнойный сепсис сопровождается массивным поступлением патогенных микроорганизмов в циркулирующую кровь из гноящегося воспалительного очага, поэтому течение заболевания отличается выраженной тяжестью и интенсивностью клинических проявлений. При условии отсутствия своевременной адекватной противовоспалительной терапии, сепсис крови в 90% случаев заканчивается летально.
В качестве этиологического провокатора воспалительной реакции и дальнейшего развития клинического симптомокомплекса сепсиса может выступать практически любой патогенный для человека микроорганизм, а также простейшие, грибы и вирусные частицы. Патогенез сепсиса запускается при попадании в общий кровоток первой порции токсинов.
Сепсис у детей протекает с выраженной системной воспалительной реакцией и крайне негативно влияет на состояние здоровья пациента.
Если рассматривать терминологию, то диагноз сепсис в переводе с греческого означает «гниение». Независимо от клинической и этиопатогенетической формы сепсиса, клиническая картина заболевания быстро прогрессирует и ни при каких условиях не может закончиться спонтанным выздоровлением. Даже, при условии применения современных методов лечения, сепсис крови отличается высоким уровнем летальности и имеет неблагоприятный прогноз в отношении выздоровления.
Следует учитывать, что развитие сепсиса у человека в большинстве ситуаций не зависит от концентрации или патогенности вируса и имеется прямая корреляционная зависимость активности септического процесса от функции иммунного аппарата человека. Так, один и тот же тип возбудителя у человека с достаточной работой иммунной системы провоцирует развитие кратковременного ограниченного воспалительного процесса, а у лиц с иммунодефицитом становится причиной развития сепсиса.
Особую группу риска по развитию сепсиса составляют пациенты в послеоперационном периоде, а также лица, находящиеся на иммуносупрессивной медикаментозной терапии. Кроме того, в качестве провокатора развития сепсиса следует рассматривать поступление микроорганизмов при катетеризации вены. Отдельного рассмотрения заслуживает такая форма заболевания как острый сепсис, возникающий в послеродовом и послеабортивном периоде, развивающийся в результате попадания инфекционного агента в организм женщины через открытую раневую поверхность матки.
В зависимости от этиопатогенеза, источника инфекции, локализации первичного инфекционного очага, активности нарастания клинической симптоматики различают разнообразные формы сепсиса, каждую из которых обязательно необходимо выносить в диагноз.
Причины сепсиса
Сепсис у взрослого пациента или ребенка развивается в результате массивного инфицирования токсинами и продуктами гнилостной деструкции патогенных микроорганизмов, при применении неадекватной схемы лечения основного заболевания, то есть данную патологию специалисты рассматривают как генерализацию воспалительного процесса. Диагноз «сепсис» представляет собой крайне опасное для человека состояние, которое часто заканчивается летальным исходом.
Даже несмотря на бурное развитие фармацевтической промышленности и внедрения новых технологий в лечении инфекционных заболеваний, инфекционный сепсис представляет собой актуальную медико-социальную проблему. В лечении сепсиса используются различные высокоактивные антибактериальные препараты последнего поколения и вместе с тем, данная патология является лидирующей среди причин летального исхода у пациентов инфекционного профиля.
Среди основных этиопатогенетических провокаторов развития сепсиса следует рассматривать бактериальную кокковую флору, синегнойную палочку, грибы, вирусы и простейшие. Патогенез сепсиса развивается при сочетании таких звеньев как: попадание в организм человека активного возбудителя инфекции, длительное течение воспалительного процесса в первичном очаге инфекции и повышенная индивидуальная реактивность организма человека.
Риск провокации сепсиса значительно увеличивается при высокой концентрации возбудителя инфекции в первичном воспалительном очаге, после чего большая масса вирусных частиц или бактериальной флоры попадает в общий кровоток. Немаловажное значение имеет состояние индивидуальной резистентности организма пациента, которая может значительно подавляться в результате воздействия разнообразных неблагоприятных факторов. В качестве негативных факторов, провоцирующих подавление работы иммунного аппарата человека, следует рассматривать тяжелую соматическую патологию, эндокринные нарушения, онкопатологию, изменение качественного и количественного состава крови, иммунологические нарушения, хроническую витаминную недостаточность, психоэмоциональную нагрузку и пролонгированный прием лекарственных средств группы иммуносупрессоров и кортикостероидов.
Основным звеном патогенеза развития сепсиса является распространение инфекционных агентов из первичных воспалительных очагов через кровеносные и лимфатические коллекторы с дальнейшим формированием вторичных септических метастазов, которые также усиливают процесс воспаления. Патоморфологическим субстратом сепсиса является образование множества гнойников различной локализации.
Развитие генерализации инфекционного процесса при сепсисе обусловлено преобладанием токсического влияния возбудителя на организм над бактериостатическими свойствами факторов иммунной защиты. Развитие сепсиса возможно не только при массивном срыве иммунитета, а даже при нарушении работы какого-либо звена в работе иммунного аппарата человека, что сопровождается нарушением выработки антител, снижением фагоцитарной активности макрофагов, а также подавлению активности лимфоцитов.
Классификация сепсиса
В большинстве ситуаций развития сепсиса известным является первичный очаг воспалительного процесса, исключение составляет лишь раневой сепсис, который также довольно распространен. Все этиопатогенетические варианты сепсиса развиваются на фоне сниженной работы иммунного аппарата человека, благодаря чему создаются благоприятные условия для диссеминации возбудителя.
Разделение сепсиса на различные формы производится специалистами на основании имеющихся анамнестических данных. Так, в зависимости от происхождения первичного воспалительного очага распространения инфекции выделяются разнообразные формы сепсиса. При хирургическом сепсисе в качестве первичного инфекционного очага выступает нагноенная рана или ограниченные гнойники. Акушерско-гинекологический сепсис развивается при нарушении технологии и санитарных нормативов во время родоразрешения или медицинского аборта, вследствие чего раневая поверхность матки является благоприятной поверхностью для размножения инфекционных агентов. Урологический гнойный сепсис имеет место у пациентов, страдающих хронической задержкой мочи, сопровождающейся развитием изменений воспалительного характера. К редким этиопатогенетическим формам сепсиса относятся риногенный, отогенный и тонзилогенный, при которых ворота инфекции расположены в ЛОР- органах.
В зависимости от патогенетических механизмов развития сепсиса выделяется септицемическая форма заболевания, при которой не формируются метастатические очаги гнойной инфекции, и септикопиемическая, отличающаяся генерализацией патологического процесса глубоким распространением инфекции.
Учитывая интенсивность нарастания клинических и лабораторных маркеров сепсиса, данная патология может протекать в молниеносной (несколько суток), острой (до одной недели), подострой (менее 6 недель) и хронической (более 6 недель) форме. Хронический сепсис относится к категории редких инфекционных патологий, склонных к частому рецидивированию.
Симптомы и признаки сепсиса
Течение сепсиса может сопровождаться развитием полиморфной клинической симптоматики, проявления которой часто симулируют клиническую картину других заболеваний и патологических состояний. Стертая клиническая картина сепсиса в большинстве ситуаций обусловлена применением интенсивной антибиотикотерапии, которая, к сожалению, не сопровождается тотальной гибелью возбудителя. Атипичность клинической картины сепсиса в этой ситуации заключается в развитии патогенеза заболевания при невыраженной пиретической реакции. Главным патогномоничным клиническим маркером сепсиса является гектическая лихорадка, сопровождающаяся обильным потоотделением, скачкообразным пульсом и артериальным давлением, ознобом и головной болью, общей слабостью, рвотой и поносом, утратой аппетита, обезвоживанием и стремительной потерей веса.
При объективном осмотре пациента, страдающего сепсисом, обращает на себя внимание землистая окраска кожных покровов со снижением ее эластичности и тургора, а также наличие распространенных подкожных флегмон и абсцессов.
Сепсис у детей на ранних стадиях развития провоцирует нарушения психоэмоционального состояния вплоть до формирования грубой неврологической симптоматики и глубокого нарушения сознания. Хронический сепсис провоцирует развитие медленно-прогрессирующей полиорганной недостаточности с появлением характерных патоморфологических изменений в различных внутренних органах.
Клиническими критериями начинающегося ДВС-синдрома, как самого распространенного варианта осложненного течения сепсиса, является появление обильной сыпи геморрагического характера, неспецифической распространенной миалгии, дыхательных нарушений, как косвенного признака интерстициального отека легких.
Клиническим критерием перемены возбудителя при сепсисе является резкое ухудшение состояния, проявляющееся быстрым повышением температуры тела, ознобом, нарастающим лейкоцитозом. Зачастую такие изменения сопутствуют септикопиемической полости.
Диагностика сепсиса
Установление диагноза «сепсис» на долабораторном этапе становится возможным при условии адекватной оценки имеющейся у пациента клинической симптоматики, при условии ее типичного развития. Кроме того, следует учитывать анамнестические данные, которые предшествовали развитию клинической картины сепсиса (послеоперационный период, ранение и тяжелые формы инфекционного заболевания).
При оценке результатов гемограммы пациента, страдающего сепсисом, обращает на себя внимание выраженный лейкоцитоз с явным палочкоядерным сдвигом формулы влево на фоне абсолютной тромбоцитопении. С целью идентификации возбудителя сепсиса следует применять бактериологическое исследование его гемокультуры, который должен производиться трехкратно с периодичностью в один час до употребления антибактериальных препаратов.
Оценивая тяжесть состояния пациента, страдающего какой-либо этиопатогенетической формой сепсиса, следует в первую очередь учитывать его индивидуальный «системный воспалительный ответ», который представляет собой системную реакцию организма на влияние активного инфекционного агента. Отличительным признаком сепсиса в этой ситуации является генерализация патологического воспалительного процесса со склонностью к развитию множественных ограниченных очагов воспаления.
В качестве инструментальных дополнительных методов визуализации сепсиса следует использовать различные методы лучевой диагностики в виде рентгенографии, ультразвукового исследования и компьютерной томографии. Так, при локализации септических проявлений в костной ткани у пациента появляются рентгенологические признаки остеомиелита в виде развития ограниченных или протяженных участков деструкции кости. При полиорганном поражении воспалительным и инфекционным процессом сепсис достаточно быстро диагностируется на УЗИ и томографических сканограммах в виде скиалогических признаков внутрибрюшных и внутригрудных абсцессов, неограниченных инфильтратов.
При тяжелом течении сепсиса у пациента появляются признаки сердечно-сосудистой недостаточности в виде гипотензии и гипоперфузии. Биохимические лабораторные нарушения возникают, как правило, в терминальной стадии сепсиса и являются отображением полиорганной недостаточности.
Лечение сепсиса
Определение объема и специфичности терапии сепсиса должно производиться на основании особенностей патогенеза развития заболевания. Основополагающим звеном терапии сепсиса является применение различных методик, купирующих проявления ДВС-синдрома и предотвращающих дальнейшее распространение инфекционных и воспалительных агентов по организму. Все пациенты, у которых течение клинической картины основного заболевания осложнилось развитием сепсиса, подлежат незамедлительной госпитализации в палату реанимационного отделения для проведения интенсивной терапии, так как течение данной патологии крайне агрессивное и склонно молниеносному развитию летального исхода. При несвоевременном применении препаратов патогенетического значения сепсис может осложняться кровоизлиянием в надпочечники, гангреной конечностей, необратимыми изменениями внутренних органов.
После проведения экспресс-метода определения чувствительности возбудителя инфекции, необходимо в незамедлительном порядке начинать массивную антибактериальную терапию в максимально допустимых дозах препарата. При имеющихся клинических и лабораторных признаках ДВС-синдрома оправдано проведение активного плазмафереза, для чего у пациента производится забор 1,5 л плазмы и внутривенно вводится около 1 л свежезамороженной плазмы. Тяжелое течение сепсиса является основанием для увеличения объема вводимой свежезамороженной плазмы, но не более двух литров. Проведение плазмафереза должно сочетаться с гепаринотерапией (суточная доза для взрослого человека составляет 40000 Ед). Предпочтительным способом введения Гепарина в этой ситуации является парентеральный.
При развитии у пациента, страдающего сепсисом, артериальной гипотензии следует использовать препараты группы симпатомиметиков, однако, при выраженной гипотензии препаратом первой линии является Преднизолон однократно. Пролонгированный прием кортикостероидной терапии является крайне неблагоприятным при сепсисе, за исключением имеющегося кровоизлияния в надпочечники. Наличие у пациента признаков артериальной гипотензии не является противопоказанием для проведения плазмафереза, однако, объем вводимой свежезамороженной плазмы следует уменьшить до 500 мл.
В большинстве ситуаций провести экстренный анализ чувствительности флоры к различным группам антибактериальных препаратов не представляется возможным, поэтому следует проводить так называемую эмпирическую антибактериальную терапию, заключающуюся в сочетании Гентамицина в суточной дозе 160 мг и Цефалоридина в суточной дозе 4 г с предпочтительным парентеральным способом введения. Объективными критериями, свидетельствующими об эффективности проводимой антибактериальной терапии, является улучшение субъективного состояния пациента, стабилизация гемодинамических нарушений, снижение температуры тела, исчезновение озноба, уменьшение интенсивности сыпи. Лабораторными критериями положительной эффективности антибактериального лечения является снижение концентрации палочкоядерных элементов и в целом устранение показателей воспаления.
В ситуации, когда возбудителем сепсиса является анаэробная флора, препаратом выбора является Метронидазол по 500 мг в сутки, а при грибковой инфекции – Флуконазол в суточной дозе 200 мг. С целью улучшения работы иммунного аппарата пациента, целесообразным является применение Иммуноглобулина с предпочтительным внутривенным введением.
С целью восстановления адекватной перфузии, нормализации клеточного метаболизма, коррекции расстройств гомеостаза, снижения концентрации медиаторов воспаления и токсических метаболитов следует с первых часов пребывания пациента в стационаре начинать инфузионную терапию, подразумевающую применение кристаллоидных и коллоидных растворов. Коррекция выраженного дефицита объема циркуляционной крови производится посредством применения декстранов, гидроксиэтилкрохмала.
Осложнения и последствия сепсиса
При генерализованном сепсисе у пациента в первую очередь развиваются осложнения гемодинамического и дыхательного характера ввиду резкого падения РаО2 и повышения проницаемости аэрогематического барьера. Результатом вышеперечисленных изменений является пропотевание жидкостного компонента в альвеолы, провоцирующее нарушение газообменной функции легких. Рентгенологическими признаками развития шокового легкого является прогрессирующая инфильтрация легочных полей двухсторонней локализации, что наблюдается практически у 20% больных при сепсисе. Клиническая симптоматика шокового легкого при сепсисе аналогичная той, что развивается при пневмонии вирусной или пневмоцистной природы.
При резком падении ОПСС и снижении объема циркулирующей крови развивается патогенез септического шока. Среди провокаторов его развития следует отметить усиление проницаемости сосудистой стенки капилляров и последующий выход жидкостного компонента из сосудистого русла. Прогрессирование септического шока, как варианта осложнения сепсиса, наблюдается при обезвоживании, что характерно для большинства фоновых инфекционных заболеваний. В дебюте септического шока у пациента не отмечается нарушение сердечного выброса или наблюдается его компенсаторное увеличение, что позволяет проводить дифференциальную диагностику с кардиогенным, обструктивным и гиповолемическим шоком.
Гемодинамические нарушения при септическом шоке дебютируют спустя одни сутки и заключаются в развитии увеличения конечно-диастолического и конечно-систолического объема с уменьшением фракции выброса. Развитие летального исхода септического шока происходит скорей не от гемодинамических нарушений, а от полиорганной недостаточности.
Негативное влияние сепсиса оказывается и на почки, что лабораторно проявляется олигурией, азотемией, протеинурией и цилиндрурией. Развитие почечной недостаточности при сепсисе имеет место в результате повреждения почечных капилляров и канальцевого некроза. У части пациентов на фоне сепсиса отмечается развитие гломерулонефрита, интерстициального нефрита, кортикального некроза почек.
В 50% случаев сепсиса отмечается развитие разнообразных нарушений свертывания крови, обусловленных тромбоцитопенией, что является главным провокаторным фактором в развитии ДВС-синдрома.
Хронический сепсис осложняется, как правило, полинейропатией, установление которой становится возможным только после применения электрофизиологических методов исследования. Появление симптоматики полинейропатии у пациента с сепсисом требует проведения дифференцировки с синдромом Гийена-Барре , метаболическими нарушениями и токсическим поражением нервной системы.
Профилактика сепсиса
Основополагающим звеном в предупреждении развития сепсиса является проведение своевременной диагностики инфекционно-воспалительных процессов в организме человека и назначении адекватной схемы терапии. Подбор терапии должен основываться в первую очередь на этиологическом факторе возникновения инфекции, что становится возможным при условии проведения анализа на чувствительность флоры. Лечащим специалистам обязательно необходимо проводить разъяснительную работу о вреде самолечения и необходимости своевременного выявления инфекционных и других воспалительных процессов, происходящих в организме.
При ведении пациента, страдающего даже ограниченным гнойным воспалительным процессом (панариций, фурункул), следует учитывать, что он является потенциальным пациентом для развития сепсиса. В этой связи оперативное лечение пациента должно подкрепляться назначением медикаментозной противовоспалительной и противомикробной терапии. При первичном осмотре пациента, поступившего на прием вследствие имеющейся раневой поверхности на кожных покровах, лечащему врачу следует уделять повышенное внимание вопросам первичной хирургической обработки с соблюдением всех санитарно-гигиенических нормативов асептики и антисептики.
Ввиду учащения случаев послеродового и послеабортного сепсиса в структуре заболеваемости данной патологией, повышенное внимание гинекологов должно уделяться вопросам соблюдения санитарных нормативов в операционной. Кроме того, необходимо исключать возможность проведения медицинского аборта вне лечебного учреждения.
В качестве профилактики развития отогенного и тонзилогенного сепсиса необходимым является проведение регулярной санации ротовой полости и ушных раковин. Пациентам, у которых нарушена функция иммунного аппарата, необходимо в профилактических целях принимать курсы иммуностимуляторов растительного происхождения, так как данные лица относятся к категории риска по развитию сепсиса.
Сепсис – какой врач поможет? При наличии или подозрении на развитие сепсиса следует незамедлительно обратиться за консультацией к таким врачам как инфекционист, хирург, гематолог.
vlanamed.com
Сепсис
- это недостаточная или извращенная реакция организма в ответ на внедрение различных возбудителей, сопровождающаяся генерализацией инфекции, при этом утрачивается самостоятельная способность организма бороться с ней.
В отличие от других инфекционных заболеваний, сепсис не заразен и не имеет определенного инкубационного периода. Сепсис встречается у 1-2 из 1000 хирургических больных, в отделениях гнойной хирургии значительно чаще – до 20%.
Сепсис в 2 раза чаще встречается у мужчин, причем в возрасте 30-60 лет. У пожилых людей и детей сепсис возникает чаще, а протекает тяжелее.
Летальность при сепсисе достигает 60%, а при септическом шоке – 90%.
1). Бактериологическая теория (Давыдовский, 1928 г.): все изменения в организме являются следствием попадания микроорганизмов в кровь.
2). Токсическая теория (Савельев, 1976 г.): все изменения вызывают экзо- и эндотоксины микроорганизмов.
3). Аллергическая теория (Ройкс, 1983 г.): токсины микроорганизмов вызывают аллергические реакции в организме.
4). Нейротрофическая теория (Павлов и его последователи): основное значение отдается в роли нервной системы в развитии изменений в организме.
5). Цитокиновая теория (Эртел, 1991 г.) наиболее полно отражает современные взгляды: микроорганизмы вызывают усиленное поступление в кровь цитокинов (т.е. веществ, регулирующих специфический и неспецифический иммунитет). Процесс начинается с выработки макрофагами фактора некроза опухоли (TNF), который вызывается секрецию интерлейкинов, что ведет к повреждению и развития синдрома системной воспалительной реакции (ССВР). Вскоре развивается угнетение иммунной системы и резко уменьшается секреция интерлейкина-2, ответственного за образование Т- и В-лимфоцитов и синтез антител.
По мнению большинства ярославских ученых, кроме сепсиса, следует выделить гнойно-резорбтивную лихорадку как процесс, предшествующий ему.
Гнойно-резорбтивная лихорадка сохраняется в течение примерно недели после вскрытия гнойного очага и характеризуется волнообразным течением, при отрицательных посевах крови на флору.
Сепсис является гораздо более тяжелой патологией. Сепсис классифицируют по следующим признакам:
1). По возникновению:
- Первичный (криптогенный) – возникает без явного гнойного очага.
- Вторичный – развивается на фоне существования гнойного или воспалительного очага в организме.
2). По локализации первичного гнойного очага:
- хирургический, гинекологический, послеродовый, сепсис новорожденных, урологический (уросепсис), терапевтический, отогенный, однотогенный и т.д.
3). По виду возбудителя:
- стафилококковый, стрептококковый, коли-бациллярный, синегнойный, анаэробный, смешанный. Выделяют также Грам-положительный и Грам-отрицательный сепсис.
4). По источнику:
- раневой, послеоперационный, воспалительный (после абсцессов, флегмон).
5). По времени развития:
- Ранний – возникает в срок до 2 недель с момента возникновения гнойного очага. Протекает по типу бурной аллергической реакции в сенсибилизированном организме.
- Поздний – возникает через 2 недели и более после возникновения первичного гнойного очага. Причиной его является возникновение сенсибилизации организма при длительно текущем местном гнойном процессе.
6). По клиническому течению:
- Молниеносный - длится 1-2 дня и обычно заканчивается смертью больного. Чаще эта форма сепсиса возникает при фурункулах и карбункулах лица. Клинически трудно отличить молниеносный сепсис от септического шока. Для последнего более характерны грубые нарушения гемодинамики.
- Острый (самая частая форма: 70-80% больных) - длится до 1-2 недель и имеет более благоприятный прогноз. Однако летальность довольно высокая.
- Подострый – длится 1-2 месяца, обычно заканчивается выздоровлением или переходит в хронический.
- Рецидивирующий – длится до 6 месяцев и характеризуется сменой периодов обострений и ремиссий. Посевы крови на флору при обострении обычно положительные.
- Хронический (хрониосепсис) – течет месяцами, иногда - годами, постепенно вызывая дегенерацию внутренних органов. Однако некоторые авторы считают, что хронического сепсиса не бывает.
7). По характеру реакций организма:
- Гиперэргический тип – в организме преобладают деструктивно-дегенерационные изменения.
- Нормэргический тип – преобладают воспалительные явления.
- Гипэргический (анэргический) тип (встречается чаще других) - вялая реакция, наблюдающаяся у ослабленных больных.
Нормэргический тип реакции чаще встречается при септикопиемии, а гипер- и гипэргический типы – при септицемии.
8). По наличию гнойных отсевов выделяют 2 формы (встречаются с примерно одинаковой частотой):
- Септицемия – протекает без гнойных отсевов. Это более тяжелая форма, характеризующаяся прогрессирующим течением.
- Септикопиемия – протекает с вторичными гнойными метастазами, что выражается периодическими обострениями, что сменяется стиханием симптоматики при вскрытии вторичных очагов.
9). По фазам развития (Ю.Н.Белокуров с соавт., 1977):
- Фаза напряжения – резкая мобилизация защитных сил организма в результате стимуляции гипофизарно-надпочечниковой системы.
- Катаболическая фаза – проявляется катаболизмом белков, жиров и углеводов; а также нарушениями водно-солевого и кислотно-щелочного равновесия.
- Анаболическая фаза – проявляется переходом метаболизма на анаболический путь. В первую очередь восстанавливаются структурные протеины.
- Реабилитационная фаза – происходит полное восстановление всех обменных процессов.
Сепсис могут вызвать практически все известные микроорганизмы – как патогенные, так и условно-патогенные. Чаще это стафилококк (50%), стрептококк, пневмококк, синегнойная палочка, протей, кишечная палочка, анаэробы (клостридиальные и неклостридиальные), грибы (кандиды). В последние годы увеличилась частота смешанного сепсиса (до 10%).
Сепсис может возникнуть:
1). При обширных ранах и открытых переломах, особенно у ослабленных и обескровленных больных. Микроорганизмы беспрепятственно попадают в кровь, т.к. не успевает развиться тканевая реакция (защитный грануляционный вал).
2). При местной гнойной инфекции, когда очаг вовремя не был вскрыт и дренирован.
3). После медицинских манипуляций – катетеризации сосудов, протезирования и др. В этом случае возбудителем часто является Грам-отрицательная внутрибольничная (назокомиальная) микрофлора.
Развитие той или иной формы сепсиса часто зависит от вида возбудителя:
- Стафилококковый сепсис обычно протекает по типу септикопиемии (90-95%) и осложняется септической пневмонией.
- Стрептококковый сепсис чаще протекает по типу септицемии (без гнойных метастазов). Метастазы возникают всего в 35% случаев.
- Синегнойный сепсис протекает по типу молниеносного с частым развитием шока.
- Анаэробный сепсис редко сопровождается гнойными метастазами, но характеризуется тяжелейшей интоксикацией и высокой летальностью.
Если первичная микрофлора, вызвавшая сепсис, может быть различной, то начиная со 2-3 недели обычно происходит смена микрофлоры на эндогенную, которая обладает большей тропностью к тканям организма и поэтому вытесняет экзогенную флору в конкурентной борьбе. В эндогенной флоре преобладают неклостридиальные анаэробы.
Предрасполагающими факторами являются:
- Повышенная вирулентность микроорганизма, устойчивость их к антибиотикам. Особенно опасны в этом плане госпитальные штаммы микроорганизмов. Бесконтрольное неправильное применение антибиотиков и иммунодепрессантов.
- Ослабленный организм человека (истощение, гиповитаминоз, сопутствующие заболевания), неспособный ограничить распространение инфекции. Сюда же относятся люди с врожденным или приобретенным иммунодефицитом, а также с гормональными заболеваниями (диабет, недостаточность надпочечников).
- Длительно существующий в организме гнойный очаг, особенно в случаях, когда он не подвергается оперативному лечению (длительное скопление гноя). Распространение инфекции их первичного гнойного очага может происходить как гематогенно, так и лимфогенно.
Развитие той или иной формы или типа клинического течения сепсиса зависит от степени взаимодействия этих 3 факторов.
Бактерии или их эндотоксины активируют систему комплемента, систему свертывания; а также нейтрофилы, моноциты, макрофаги и клетки эндотелия. Эти клетки активируют медиаторы воспаления: цитокины, фактор свертываемости Хагемана, кинины, лейкотриены, простагландины, протеолитические ферменты и свободные радикалы. В результате развивается системная воспалительная реакция, ведущая к повреждению клеток, нарушению микроциркуляции и развитию полиорганной недостаточности.
Патогномоничных симптомов сепсиса нет. Сепсис имеет множество форм и клинических проявлений, которые трудно систематизировать.
Наиболее часто источником сепсиса (т.е. первичным очагом) являются тяжелые травмы, карбункулы (особенно на лице), флегмоны, абсцессы, перитонит и др. При септикопиемии вторичные гнойные очаги (обычно это абсцессы) чаще возникают в легких, почках, костном мозге (при стафилококковом сепсисе), в суставах (при стрептококковом сепсисе), в мозговых оболочках (при пневмококковом сепсисе) и т.д.
Наиболее типичной является картина острого сепсиса:
1). Общие симптомы:
- Повышение температуры до 40 оС и более, сопровождающееся ознобом – 2-7 раз в сутки. При сепсисе наблюдается 2 основных типа лихорадки: ремиттирующая (при септицемии) - размах температурной кривой обычно не более 2 оС; волнообразная (при септикопиемии) – повышение температуры после образования вторичных метастазов сменяется ее падением после их вскрытия и дренирования. При хроническом сепсисе лихорадка становится нерегулярной, а при истощении больного – температура снижается.
- Холодный обильный липкий пот.
- Недомогание, слабость.
- Потеря аппетита, иногда - профузный понос.
- Иногда, в тяжелых случаях, наблюдаются психические нарушения: от полной апатии до психозов, галлюцинаций и беспричинной эйфории.
2). Внешний вид:
- Лицо вначале гиперемировано, но по мере прогрессирования сепсиса становится осунувшимся, землистого цвета, иногда наблюдается иктеричность склер и кожи (у 25% больных).
- Кожа может приобрести мраморный оттенок – из-за нарушения микроциркуляции.
- Язык сухой, потрескавшийся, обложен налетом.
- На теле часто выявляются петехии на коже и слизистой полости рта, на губах может наблюдаться герпес.
- При септикопиемии под кожей могут появляться мелкие абсцессы (вторичные гнойные метастазы).
- Часто развиваются пролежни.
3). Симптомы поражения сердечно-сосудистой системы:
- Тахикардия.
- Артериальное давление нормальное или слегка снижено. При септическом шоке АД может упасть до критического – в этом случае прекратится фильтрация мочи.
- При аускультации сердца может выслушиваться диастолический шум над аортой.
- Септикопиемия может осложниться эндокардитом и эмболиями большого круга кровообращения.
4). Симптомы поражения ЖКТ:
- Паралитическая кишечная непроходимость.
- Увеличение размеров печени и селезенки. Симптомы печеночно-почечной недостаточности обычно обнаруживают лабораторными методами (см. ниже).
5). Симптомы дыхательной недостаточности:
- Обтурационная ДН проявляется тахипноэ, цианозом, тахикардией, повышением АД.
- При септическом шоке ДН протекает по типу респираторного дистресс-синдрома с последующим развитием отека легких.
- В легких часто обнаруживаются вторичные гнойные отсевы.
6). Состояние первичного гнойного очага при сепсисе имеет некоторые особенности. Гнойный очаг при сепсисе реагирует первым, еще до развития тяжелого общего состояния:
- Грануляции - вялые, бледные, при дотрагивании – легко кровоточат.
- Быстрое прогрессирование некротических изменений.
- Некротизированные ткани отторгаются крайне медленно.
- Раневое отделяемое скудное, приобретает геморрагический или гнилостный характер.
- Ткани вокруг очага отечны, имеют бледно-синюшный оттенок.
Если при аэробном сепсисе границы гнойного очага хорошо определяются на глаз, то при анаэробном внешне очаг может выглядеть неплохо, но на самом деле инфекция уже распространилась далеко по жировой клетчатке и межфасциальным промежуткам.
Дополнительные методы исследования при сепсисе:
1). Общий анализ крови:
- Лейкоцитоз (до 15-20 х 109/л) со сдвигом влево, токсическая зернистость лейкоцитов, увеличение лейкоцитарного индекса интоксикации (ЛИИ), относительная лимфопения.
- Резкое ускорение СОЭ – до 60-80 мм/ч (что не соответствует лейкоцитозу).
- Прогрессирующая анемия (снижение гемоглобина до 70-80 г/л).
- Прогрессирующая тромбоцитопения.
2). Биохимический анализ крови
- выявляет признаки печеночно-почечной недостаточности:
- Уменьшение уровня неорганического фосфата.
- Увеличение уровня и активности протеолитических ферментов (трипсина, химотрипсина).
- Увеличение уровня лактата (особенно при анаэробном сепсисе).
- Увеличение уровня “средних молекул” (пептидов с массой 300-500 Дальтон).
- Увеличение уровня креатинина.
- Увеличение уровня билирубина, АСТ и АЛТ.
- Дефицит белка (т.к. потери белка при сепсисе могут достигать 0,5 г в сутки).
- Измерение уровня цитокинов позволяет оценить тяжесть процесса и его стадию.
3). Общий анализ мочи: у 20% больных развивается почечная недостаточность: определяется олигоурия, протеинурия; а также эритроцитурия, лейкоцитурия, цилиндрурия.
4). Посев крови на наличие микроорганизмов ( = посев на флору, посев на стерильность) – берут 3 дня подряд (на высоте озноба или сразу после него). Результат посева становится известен только примерно через неделю. Отрицательный результат не противоречит диагнозу сепсиса (т.к. это часто наблюдается на фоне антибактериальной терапии). В то же время наличие микроорганизмов в крови не говорит о сепсисе, для постановки такого диагноза необходима соответствующая клиника. А бактериемия может встречаться и без сепсиса (например, при брюшном тифе, роже, остром остеомиелите).
Бактериологическому исследованию подвергаются также моча, мокрота и раневое отделяемое из гнойного очага.
5). Коагулограмма: увеличение времени свертываемости крови.
6). Иммунограмма: снижение количества Т-лимфоцитов – особенно характерно для анаэробного сепсиса. Снижается продукция антител (особенно классов M и G).
7). Специальными методами можно выявить повышение в крови концентрации:
- Иммунных комплексов.
- Продуктов свободнорадикального окисления (масляный альдегид, изовалериановый альдегид и др.).
1). Септический (инфекционно-токсический) шок.
2). Септические кровотечения - развиваются в результате:
- Гнойного расплавления сосуда в гнойном очаге (аррозивные кровотечения).
- Нарушения проницаемости стенки сосудов (диапедезные кровотечения).
- Пролежня стенки сосуда дренажем.
Способствует кровотечению и нарушения в системе гемостаза при сепсисе.
3). Септический эндокардит (чаще поражается митральный клапан). Часто возникают септические тромбы на клапанах, которые могут вызвать тромбоэмболию артерий конечностей или внутренних органов и привести к гангрене конечностей или инфаркту внутренних органов.
4). Септические пневмонии, часто – абсцедирующие.
5). Пролежни.
Септический шок
- это реакция организма на массивный прорыв в кровь микроорганизмов или их токсинов, что проявляется острой сосудистой недостаточностью:
- Резкое падение артериального давления до критического.
- Частый слабый аритмичный пульс.
- Кожные покровы бледные.
- Выраженый акроцианоз, одышка (до 40 в минуту).
- Из-за падения давления прогрессирует олигурия вплоть до анурии.
В течении септического шока выделяют фазы компенсации, субкомпенсации и декомпенсации.
Грам-отрицательный сепсис осложняется септическим шоком в 20-25%, граммположительный - только в 5% случаев.
Возникновение шока при сепсисе значительно утяжеляет состояние больного и ухудшает прогноз заболевания – летальность до 90%.
Наиболее частые причины смерти при сепсисе:
1). Септическая пневмония.
2). Прогрессирующая интоксикация.
3). Прогрессирующая печеночно-почечная недостаточность.
4). Развитие гнойных метастазов в жизненно-важных органах (сердце, легких, печени, почках).
5). Острая сердечная недостаточность (как результат поражения клапанов сердца).
Критерии диагностики сепсиса были разработаны в 1991 г. на “конференции согласия” с участием ведущих ученых-септологов мира.
1). Симптомы системной воспалительной реакции (ССВР):
- Температура выше 38 оС или ниже 36 оС.
- Тахикардия больше 90 в минуту.
- Частота дыхания чаще 20 в минуту (или снижение парциального давления углекислого гага в крови меньше 32 мм рт.ст.).
- В анализе крови – лейкоцитоз более 12 х 109/л или менее 4 х 109/л (или число незрелых форм превышает 10%).
2). Симптомы органной недостаточности:
- Легкие: необходимость ИВЛ или оксигенотерапии для поддержания парциального давления кислорода выше 60 мм рт.ст.
- Печень: уровень билирубина выше 34 мкмоль/л; или уровень АСТ и АЛТ в 2 раза превышает норму.
- Почки: повышение креатинина более 0,18 ммоль/л (или олигоурия менее 30 мл/час).
- Сердечно-сосудистая система: падение АД ниже 90 мм рт.ст., требующее медикаментозной терапии.
- Система гемостаза: снижение уровня тромбоцитов менее 100 х 109/л.
- Желудочно-кишечный тракт: паралитическая кишечная непроходимость, не поддающаяся медикаментозной терапии более 8 часов.
- ЦНС: заторможенность или сопор (при отсутствии ЧМТ или нарушений мозгового кровообращения).
Диагноз сепсиса ставится на основании:
1). Наличия первичного гнойного очага.
2). Наличия не менее 3 признаков ССВР.
3). Наличие хотя бы одного признака органной недостаточности.
Развернутый диагноз сепсиса должен включать в себя:
- Первичный источник сепсиса (гнойный очаг).
- Течение сепсиса (молниеносное, острое и т.д.), его форма (септицемия и т.д.), фаза (напряжения и т.д.).
- Осложнения.
следует проводить с брюшным и сыпным тифом, милиарным туберкулезом, бруцеллезом, малярией, а также с гнойно-резорбтивной лихорадкой.
Гнойно-резорбтивная лихорадка – это синдром, вызванный всасыванием в кровь продуктов гнойного распада тканей и бактериальных токсинов из очага острой гнойной инфекции, и проявляющийся длительной температурной реакцией. Основными отличиями гнойно-резорбтивной лихорадки от сепсиса являются следующие признаки:
- Степень тяжести гнойно-резорбтивной лихорадки соответствует местным изменениям в гнойном очаге, в то время как при сепсисе может наблюдаться тяжелейшее общее состояние при невыраженных местных изменениях.
- После вскрытия и ликвидации гнойного очага явления гнойно-резорбтивной лихорадки исчезают (не более чем через неделю), чего не наблюдается при сепсисе, при котором происходит лишь некоторое улучшение состояния.
- Посевы крови стерильны, а при сепсисе часто наблюдается бактериемия.
Лечение сепсиса
Лечение сепсиса должно быть как общим, так и местным (ликвидация гнойного очага). Обязательно восполняют возросшие энергозатраты организма путем полноценным питанием – как энтеральным, так и парентеральным (4000-5000 ккал/сут).
Общее лечение складывается из 5 направлений:
1). Антибиотикотерапия при сепсисе имеет свои особенности:
- Сначала назначаются бактерицидные антибиотики широкого спектра действия (ампиокс, гентамицин, линкомицин, цефалоспорины). Лучше использовать комбинацию из 2-3 антибиотиков с разным механизмом и спектром действия, причем 1 из них обязательно нужно вводить внутривенно. При неэффективности (т.е. при отсутствии улучшения в течение 3-5 дней) применяют антибиотики резерва (ципробай, тиенам). После определения возбудителя антибиотик назначаю согласно его чувствительности.
- Антибиотики при сепсисе вводят только парентерально (внутримышечно, внутривенно, внутриартериально, эндолимфатически) и местно.
- Антибиотики вводят в максимальных дозировках.
- Антибиотики лучше комбинировать с сульфаниламидами, нитрофуранами, диоксидином и метрогилом.
- Отменяют антибиотики не менее чем через 2 недели после клинического выздоровления и 2-3 подряд отрицательных посевов крови на стерильность.
2). Детоксикационная терапия:
- Обильное питье и инфузионная терапия - физраствор, 5% глюкоза с инсулином (1 ЕД инсулина на 5 г сухой глюкозы), гемодез (не более 400 мл/сут), реополиглюкин. Суточный объем вводимой жидкости может достигать 3-6 литров. Часто применяется метод форсированного диуреза (введение инфузионных растворов сочетают с мочегонными препаратами). При септическом шоке применяют правило 3 катетеров (в подключичную вену для инфузий, в мочевой пузырь для контроля за диурезом, в нос для оксигенотерапии). Обязателен контроль диуреза: количество вводимой жидкости не должно превышать количество мочи более чем на 1 л, т.к. это опасно развитием отека легких и синдрома шокового легкого. Для профилактики этих осложнений применяют инфузию растворов альбумина.
- При сепсисе широко применяются методы экстракорпоральной детоксикации: гемосорбция, плазмосорбция, плазмаферез, УФО крови, внутрисосудистая лазерная кавитация крови (ВЛОК), электрохимическое окисление крови (введение гипохлорита натрия внутривенно), гемоспленоперфузия (перфузия крови через ксеноселезенку).
- ГБО-терапия - повышает интенсивность обезвреживания токсических веществ.
3). Иммунокорригирующая терапия:
- В катаболическую фазу показана пассивная иммунизация: переливание крови, лейкомассы, плазмы (в том числе и гипериммунной), гамма-глобулин, бактерифаги, производные интерлейкина-2 (ронколейкин).
- В анаболическую фазу производят стимуляцию иммунитета: стафилококковый анатоксин, пентоксил, левамизол, продигиозан, спленин, препараты вилочковой железы (тималин, Т-активин).
4). Противовоспалительная и обезболивающая терапия:
Для обезболивания применяют анальгин, при неэффективности - наркотические анальгетики (промедол, омнопон). Из противовоспалительных средств чаще используют сильные НПВС (вольтарен, ибупрофен).
При септическом шоке НПВС обычно неэффективны. В этом случае применяют глюкокортикоиды (коротким курсом – 2-3- дня), которые обладают также и противоаллергическим действием и повышают артериальное давление. Дозировка: в первые сутки - 500-800 мг; во 2-3-е сутки – по 100-150. Однако гормоны можно применять только под контролем гормонального фона.
5). Симптоматическая терапия:
- При сердечной недостаточности - сердечные гликозиды (строфантин), кокарбоксилаза, витамин С.
- При нарушениях периферического кровообращения - но-шпа, реополиглюкин, никотиновая кислота, трентал, компламин.
- При дыхательной недостаточности - оксигенотерапия, при неэфективности - в сочетании с ИВЛ. Применяются средства, разжижающие мокроту (трипсин, ацетилцистеин) и снимающие бронхоспазм (эуфиллин).
- При гипокалиемии - вводят растворы с ионами калия внутривенно.
- При метаболическом ацидозе - бикарбонат натрия внутривенно; при алкалозе – хлорид калия, витамин С, диамокс.
- При парезе ЖКТ - одновременно со стимуляцией кишечника проводят парентеральное питание (концентрированные растворы глюкозы, жировые эмульсии, белковые гидролизаты и смеси аминокислот, витамины).
- При печеночно-почечной недостаточности – гепатопротекторы (карсил, легалон), альбумин, витамины группы В и С в больших дозах.
- При нарушениях свертываемости крови - контрикал, препараты кальция, тиосульфат натрия, гепарин.
- При истощении - в анаболическую фазу применяют анаболические гормоны (ретаболил) и увеличивают количество белков в пище.
Особенности местного лечения (вскрытия гнойного очага) при сепсисе:
1). Необходимо широкое вскрытие очага.
2). Удаление всех некротизированных тканей, вплоть до ампутации конечности или удаления целого органа. При анаэробном сепсисе рекомендуется как можно более широкое вскрытие очага и иссечение всех некротизированных тканей, при аэробном сепсисе – менее широкое (чтоб избежать раневого истощения).
3). После операции обязательна иммобилизация.
4). В послеоперационном периоде применяют ультразвуковую кавитацию, лазерное облучение раны, обработку раны пульсирующей струей антисептика.
5). Широкое адекватное дренирование.
В настоящее время существуют 2 тактики лечения послеоперационных ран при сепсисе:
- Открытый метод (наиболее распространенный) - рану дренируют, но не зашивают. В дальнейшем она заживает вторичным натяжением под повязками. Преимуществом этого способа является возможность дальнейшего динамического наблюдения за состоянием раны, недостатком - травматичность перевязок и возможность реинфицирования раны или распространения инфекции по стационару. Местное лечение производится соответственно принципам терапии гнойных ран. Лучше лечение ран открытым способом проводить в палатах с управляемой абактериальной средой (гнотобиологическая защита).
- Закрытый метод - применяют глухое зашивание раны с оставления трубчатых дренажей для проточно-промывного и вакуумного дренирования. преимуществами метода является профилактика раневого истощения и уменьшение соприкосновения раны с внешней средой. Однако наблюдать за такой раной невозможно.
Профилактика сепсиса
заключается в ранней полноценной первичной хирургической обработке ран с последующим местным и общим лечением, а также своевременное оперативное лечение местное гнойной инфекции.
dendrit.ru